Научно-производственный рецензируемый журнал «Разработка и регистрация лекарственных средств» - актуальное бесплатное прикладное издание и информационный портал для специалистов, задействованных в сфере обращения лекарственных средств. Журнал предназначен для фармацевтических предприятий-производителей и их сотрудников из отделов разработки, контроля качества, регистрации, производства и развития; сотрудников лабораторных центров, контрактно-исследовательских организаций, научных и образовательных учреждений. Индексируется в российских и международных реферативных и полнотекстовых базах, включен в наукометрические базы данных РИНЦ и Scopus, входит в "Белый список" научных изданий и Перечень ВАК (категория К1) и Russian Science Citation Index (RSCI).
Наименование и содержание научных работ, публикуемых в журнале «Разработка и регистрация лекарственных средств», должно соответствовать отраслям науки:
- 3.3.6. – фармакология, клиническая фармакология (медицинские науки, фармацевтические науки, биологические науки);
- 3.4.1. – промышленная фармация и технология получения лекарств (фармацевтические науки);
- 3.4.2. – фармацевтическая химия, фармакогнозия (фармацевтические науки).
Основные пять тематических разделов журнала «Разработка и регистрация лекарственных средств» включают цикл развития лекарственного средства от его создания до получения регистрационного удостоверения. Первый раздел посвящен поиску и разработке новых лекарственных средств, второй - фармацевтической технологии и рассматривает научные и практические направления от разработки и производства исходных фармацевтических ингредиентов, технологий и оборудования – до создания стандартных и терапевтически эффективных лекарственных препаратов. Третий раздел описывает аналитические методики контроля качества; четвертый раздел посвящен подходам к оценке эффективности и безопасности лекарственных средств, проведению долклинических и клинических исследований; в пятом разделе рассматриваются вопросы валидации методик, подготовки регистрационного досье, жизненный цикл лекарственного препарата в GxP окружении.
Текущий выпуск
ОТ РЕДАКЦИИ
Двухдневный XIX конгресс «Разработка и регистрация лекарственных средств» прошел 17 и 18 февраля 2026 года в конгресс-центре Сеченовского университета в Москве.
В рамках проекта «Мнение лидеров» состоялся открытый диалог двух экспертов фармацевтической отрасли. Игорь Евгеньевич Шохин, генеральный директор «Центра Фармацевтической Аналитики», обсудил с доктором фармацевтических наук, профессором МГУ Борисом Борисовичем Сысуевым ключевые принципы работы учебного центра «ЦФА». Эксперты поговорили о том, как выстроить эффективное обучение для профессионалов отрасли.
В статье представлена стенограмма доклада главного инженера Главхимфармпрома Д. М. Фрайштата «О положении с производством лекарственных препаратов». Доклад был представлен 31 июля 1943 года на заседании Фармакологического комитета Ученого медицинского совета Наркомздрава Союза ССР. В докладе перечислены потери, которые понесла отечественная химико-фармацевтическая промышленность в первые месяцы войны, и ее состояние к середине 1943 года. Подробно перечислены лекарственные средства, выпуск которых уже налажен на восстановленных и заново построенных предприятиях отрасли. Отмечены трудности, влияющие на рост производства лекарств, озвучены планы по введению новых производств, призванных не только увеличить выпуск традиционного ассортимента лекарственных средств, но и освоить выработку новых препаратов. Основной доклад дополнили представители Главмедфармпрома и Главного аптечного управления. Основное внимание они обратили на планы работы в 1944 году. Материалы совещания планируется представить на конференции фармакологов, терапевтов, представителей товаропроводящей цепи и представителей промышленных организаций для планирования дальнейших действий промышленности в направлении как увеличения ассортимента выпускаемых лекарственных препаратов, так и роста их тоннажного производства.
Для любой аналитической лаборатории важны эффективность и универсальность программного обеспечения. Рост ассортимента оборудования требует интегрированных решений для управления различными приборами, упрощения обучения и ускорения адаптации методов. В статье рассматривается отечественное программное обеспечение Space CDS от ГК «Лабконцепт» – современное web-приложение для автоматизации работы аналитических приборов различных производителей и типов, таких как ВЭЖХ, ГХ, спектрофотометры и ИК-Фурье спектрометры. Программное обеспечение имеет ряд существенных преимуществ в управлении, обработке данных и формировании отчетов, что облегчает его использование и подтверждает важность для современных лабораторий, работающих по стандартам GMP и ISO 17025.
ПОИСК И РАЗРАБОТКА НОВЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Введение. Многие соединения, содержащие тетразольный фрагмент, превосходят по эффективности известные противодиабетические препараты в доклинических исследованиях, а некоторые кандидаты уже находятся на стадии клинических испытаний. Широкое применение тетразольных производных для воздействия на диабет-ассоциированные мишени и терапии сопутствующих осложнений подтверждает перспективность данного каркаса для разработки новых эффективных противодиабетических средств.
Цель. Исследование (in silico, синтез, in vivo) ряда гибридных производных 5-фенилтетразола с целью выявления и последующей экспериментальной проверки перспективных соединений, обладающих гипогликемической и противожировой активностью.
Материалы и методы. Синтез гибридных гетероциклических соединений осуществлен путем ацилирования хлорангидридом (5-фенилтетразол-2-ил)уксусной кислоты ряда гетероциклических производных N-алкил-5-аминотетразола, 4-амино-4H-1,2,4-триазол-3-тиола и 2-гидразинил-4,6-диметилпиримидина.
Результаты и обсуждение. В результате in silico (PASS, докинг, скоринг) исследования биологической активности в ряду производных 5-фенилтетразола распознаны наиболее перспективные «гибридные» (полиядерные) гетероциклические соединения: N'-(4,6-диметилпиримидин-2-ил)-2-(5-фенил-2H-тетразол-2-ил)-ацетогидразид, N-(3-меркапто-4H-1,2,4-триазол-4-ил)-2-(5-фенил-2H-тетразол-2-ил)-ацетамид, N-(1-метил-1H-тетразол-5-ил)-2-(5-фенил-2H-тетразол-2-ил)-ацетамид, N-(2-метил-2H-тетразол-5-ил)-2-(5-фенил-2H-тетразол-2-ил)-ацетамид и N-трет-бутил-2-({1-[2-(5-фенил-2H-тетразол-2-ил) ацетамидо]-1H-тетразол-5-ил}тио)ацетамид. Эти соединения, по данным компьютерного прогноза, представляют интерес как потенциальные средства для фармакологической коррекции различных метаболических нарушений. Разработан и реализован рациональный метод синтеза указанных соединений, строение и индивидуальность которых доказаны с применением современных инструментальных физико-химических методов. В ходе in-vivo-исследований показано, что данные гетероциклические соединения проявляют гипогликемическую и выраженную противожировую активность.
Заключение. Проведенное исследование гибридных производных 5-фенилтетразола выявило выраженную гипогликемическую активность. Обнаружено, что гиполипидемическая активность в данном случае не связана напрямую с гипогликемическим эффектом, в отличие от закономерности, характерной для сенситайзера метформина.
Введение. Флаванонол дигидрокверцетин (ДКВ) известен выраженной антиоксидантной способностью, с которой связывают широкий спектр биологической активности данного соединения. Благодаря наличию двух центров хиральности в положениях 2 и 3 бензопиранонового кольца, для этого флавоноида характерно явление цис-транс-изомерии. Однако сопоставительный анализ антиоксидантной способности диастереомеров ДКВ ранее не осуществляли.
Цель. Оценить влияние диастереомерного состава на восстанавливающие и радикал-связывающие свойства образцов ДКВ.
Материалы и методы. Диастереомерный состав испытуемых образцов ДКВ контролировали в условиях обращенно-фазовой хроматографии с УФ-детектированием. Изучение антиоксидантной емкости осуществляли на модели ингибирования радикал-катионов 2,2'-азино-бис-(3-этилбензотиазолин-6-сульфоновой кислоты) диаммониевой соли (ABTS+•). Восстанавливающую способность образцов ДКВ оценивали на модели 5-(2,4-дисульфофенил)-3-(2-метокси-4-нитрофенил)-2-(4-нитрофенил)-2H-тетразолия мононатриевой соли (WST-8). Оба испытания проводили под контролем спектрофотомерии в УФ-области.
Результаты и обсуждение. Хроматограммы образцов, полученные при длине волны 288 нм, характеризуются двумя пиками с временами удерживания 18,79 ± 0,08 и 19,87 ± 0,08 мин, которые соответствуют транс- и цис-диастереомерам ДКВ. При добавлении к раствору ABTS•+ образцов ДКВ, содержащих 0,8, 3,7 и 9,5 % цис-изомера, оптическая плотность при 730 нм по истечении 6 мин снизилась на 0,588 ± 0,008, 0,581 ± 0,017 и 0,602 ± 0,012, соответственно (α 0,05, р 0,2196, r 0,7857), в то время как в растворах WST-8 при 450 нм для аналогичных образцов наблюдали увеличение оптической плотности на 0,178 ± 0,030, 0,222 ± 0,026 и 0,188 ± 0,036, соответственно (α 0,05, р 0,5157, r 0,0284).
Заключение. Полученные результаты свидетельствуют об отсутствии статистически значимого влияния диастереомерного состава на антиоксидантные свойства образцов ДКВ. Таким образом, наблюдаемые различия в фармакологии цис- и транс-ДКВ следует объяснять селективностью взаимодействия с биологическими мишенями, а не способностью связывать свободные радикалы.
ФАРМАЦЕВТИЧЕСКАЯ ТЕХНОЛОГИЯ
Введение. Фармацевтическая разработка представляет собой сложнейшую комплексную работу, основной целью которой является достижение целевого профиля качества продукта (Quality Target Product Profile, QTPP). QTPP формулируется на основании целого комплекса требований к препарату, включая фармакопейные, потребительские, фармакологические и пр. Традиционный эмпирический подход к разработке состава и технологии лекарственной формы в данном случае представляется трудо- и ресурсоемким, при этом не позволяет в полной мере достичь понимания всех процессов как с точки зрения технологии, так и с точки зрения дальнейших этапов жизненного цикла лекарственного препарата (ЛП). Подход «качество через проектирование» (QbD) позволяет оценить влияние факторов на процессы, что, в свою очередь, способствует проактивному управлению рисками и созданию робастных технологий.
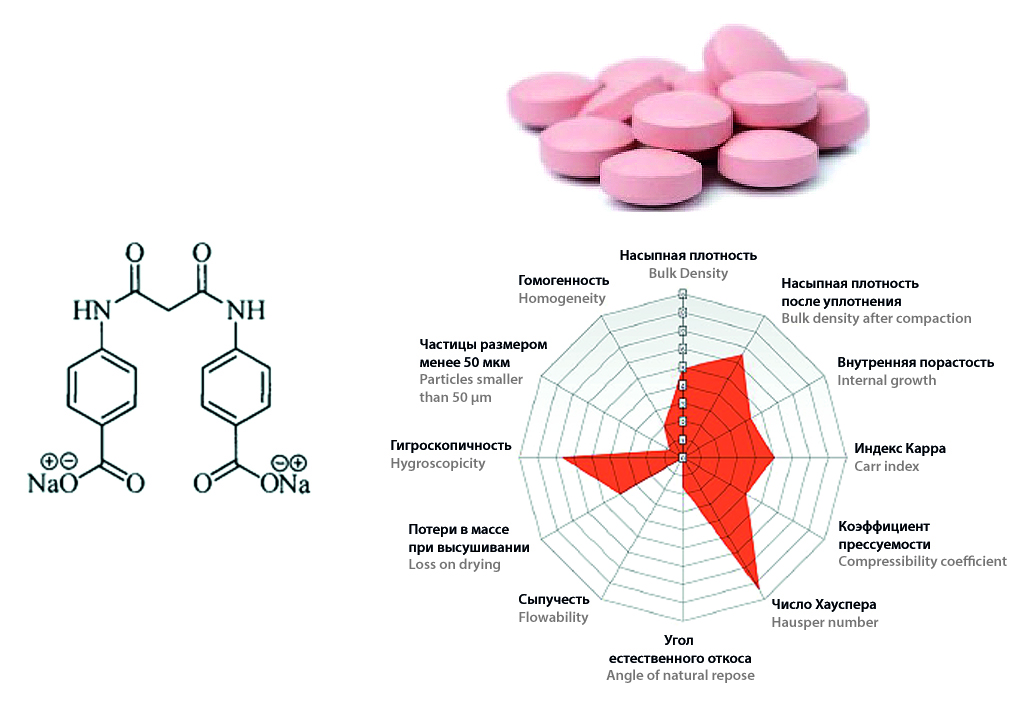
Цель. Продемонстрировать комплексное применение инструментов QbD, включая экспертные системы (Sediment Delivery Model, SeDeM), планирование экспериментов (Design of Experiment, DoE) и анализ рисков, на примере разработки состава таблеток пролонгированного действия на основе 4,4’-(пропандиамидо)дибензоата натрия.
Материалы и методы. В работе использована оригинальная активная фармацевтическая субстанция (АФС) – 4,4’-(пропандиамидо)дибензоат натрия, современные вспомогательные вещества и полимеры, обеспечивающие пролонгированное высвобождение (этилцеллюлоза, гидроксипропилметилцеллюлоза и пр.). На первом этапе для проектирования составов применялся метод SeDeM. На втором этапе для оптимизации профиля высвобождения использован скрининговый DoE.
Результаты и обсуждение. Метод SeDeM позволил количественно определить и нивелировать риски, связанные с неудовлетворительными технологическими свойствами АФС. Были спроектированы и экспериментально подтверждены составы с удовлетворительными технологическими свойствами. В результате DoE установлено, что ГПМЦ обеспечивает наиболее полное и равномерное высвобождение (более 80 % за 12 ч), приближенное к кинетике высвобождения нулевого порядка.
Заключение. Комплексное применение инструментов QbD позволило эффективно и обоснованно разработать робастный состав таблеток пролонгированного действия на основе 4,4’-(пропандиамидо)дибензоата натрия, обеспечивающий как требуемые технологические свойства, так и требуемый профиль высвобождения.
Введение. Интерполиэлектролитные комплексы (ИПЭК) – перспективные носители для систем с контролируемым высвобождением активных фармацевтических ингредиентов (АФИ). Введение АФИ ионного характера в системы доставки может приводить к образованию связей с полиэлектролитами, что оказывает влияние на высвобождение лекарственного вещества из лекарственной формы. Ранее были получены полимер-лекарственный комплекс на основе Eudragit® EPO с индометацином, а также интерполиэлектролит-лекарственный комплекс, образованный сополимерами Eudragit® EPO, Eudragit® S100 и индометацином. Проведена оценка физико-химических свойств оптимальных образцов и показана перспективность их использования в системах контролируемой доставки индометацина.
Цель. Сравнительная биофармацевтическая оценка полимер-лекарственного и интерполиэлектролит-лекарственного комплексов как систем пероральной направленной доставки индометацина.
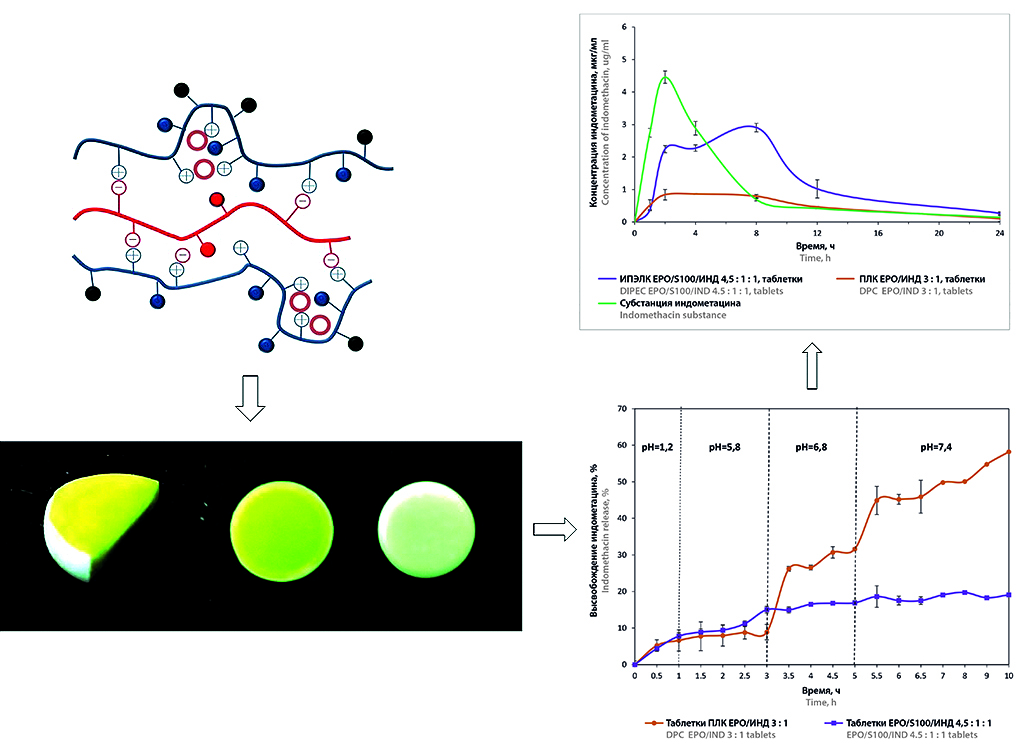
Материалы и методы. Полимер-лекарственный комплекс на основе Eudragit® EPO и индометацина (ПЛК ЕРО/ИНД) и интерполиэлектролит-лекарственный комплекс на основе Eudragit® EPO, Eudragit® S100 и индометацина (ИПЭЛК ЕРО/S100/ИНД) получены при молярном соотношении компонентов 3 : 1 и 4,5 : 1 : 1 соответственно. Оценку высвобождения индометацина из порошков и таблеток ПЛК и ИПЭЛК проводили методом II («Лопастная мешалка») с использованием тестера растворения DT 828 (ERWEKA GmbH, Германия). Концентрацию индометацина определяли УФ-спектрофотометрически на спектрофотометре Lambda 25 (PerkinElmer, США) при длине волны 270 нм. Математическое моделирование высвобождения индометацина осуществляли с использованием программы Microsoft Excel Office. Фармакокинетические исследования проводили на кроликах породы советская шиншилла. Исследуемые образцы вводили перорально, через определенные интервалы времени отбирали пробы крови из ушной вены. Концентрацию индометацина в плазме крови определяли методом ВЭЖХ на хроматографе LC-20 Prominence (Shimadzu, Япония) с УФ-детектированием. Основные фармакокинетические показатели рассчитывали с использованием программы Thermo Kinetica® (version 5.0, build 5.00.11; Thermo Fisher Scientific, США).
Результаты и обсуждение. Профили высвобождения индометацина из порошков ПЛК и ИПЭЛК характеризуются как «кишечный тип», где превалирующим механизмом является процесс релаксации полимерных цепей при высвобождении субстанции. Высвобождение индометацина из таблетированной матрицы на основе ИПЭЛК отличается от профиля высвобождения из порошка ИПЭЛК и достигает 19 %. Профиль высвобождения индометацина из таблеток ПЛК EPO/ИНД сходен с профилем высвобождения из порошка и достигает 58 %. На поверхности таблеток ИПЭЛК образуется гидрогелевый слой, который препятствует проникновению среды растворения внутрь матрицы. Высвобождение индометацина из образцов ИПЭЛК ЕРО/S100/ИНД происходит за счет диффузии лекарственного вещества из матрицы. ПЛК и ИПЭЛК в виде порошков обладают большим средним временем удерживания (MRT) по сравнению с таблетками ПЛК и ИПЭЛК. MRT ИПЭЛК и ПЛК в виде порошка превышает MRT cубстанции индометацина в три и четыре раза соответственно. Максимальная концентрация индометацина в плазме крови кроликов при пероральном введении таблеток ИПЭЛК наблюдается через 8 часов эксперимента.
Заключение. Высвобождение индометацина из ПЛК EPO/ИНД происходит за счет наличия «дефектных» областей и релаксации полимерных цепей, это обеспечивает замедленный выход АФИ и невысокую относительную биодоступность, что позволяет использовать ПЛК в системах доставки индометацина для лечения воспалительных заболеваний толстого кишечника. Таблетированные системы ИПЭЛК EPO/S100/ИНД позволяют изменить профиль высвобождения индометацина за счет процессов диффузии субстанции через образующийся гидрогелевый слой на поверхности матрицы, обеспечивая высокую биодоступность, и могут быть использованы как матричные системы для доставки АФИ в оптимальную зону всасывания.
Введение. На базе Первого МГМУ им. И. М. Сеченова (Сеченовский Университет) изготовлены образцы мягкой лекарственной формы (МЛФ), а именно гели на основе полимеров-гелеобразователей различной природы, которые содержат твердую дисперсную систему (ТДС) метронидазола (МД). При разработке составов использовались следующие полимеры: карбопол-21, аммония метакрилата сополимер, гидроксиэтилцеллюлоза, гипромеллозы фталат, ксантановая камедь и альгинат натрия. Изучено влияние полимеров на высвобождение активной фармацевтической субстанции (АФС) из разработанных МЛФ. Изготовленные гели отличаются от промышленных аналогов, представленных на российском фармацевтическом рынке не только составами, но и улучшенными биофармацевтическими свойствами. Фармацевтическая доступность МД из разработанных образцов гелей не уступает доступности промышленных аналогов, а в отдельных случаях превышает ее. В перспективе это позволит уменьшить дозировку АФС и снизить степень проявления побочных эффектов на организм.
Цель. Разработать составы и технологические схемы получения гелей на основе твердых дисперсных систем метронидазола для наружного применения с использованием полимеров-гелеобразователей различной природы.
Материалы и методы. Субстанции: метронидазол, полиэтиленгликоль-400 (ПЭГ), этилендиаминтетрауксусная кислота (ЭДТА), карбопол Ультрез-21, аммония метакрилата сополимер, гидроксиэтилцеллюлоза (ГЭЦ), гипромеллозы фталат, ксантановая камедь, альгинат натрия, гидроксид натрия, натрия бензоат, вода очищенная. Получение гелей проводилось в несколько этапов: предварительное растворение и набухание гелеобразователя; добавление нейтрализующего агента к гелеобразователю (для карбопола Ультрез-21); приготовление ТДС – раствора МД в ПЭГ; добавление хелатирующего агента – ЭДТА; перемешивание массы до образования гомогенного геля. Полученные гели исследовали согласно ОФС.1.4.1.0008 «Мягкие лекарственные формы», ОФС.1.2.1.0004 «Ионометрия» Государственной фармакопеи РФ. Срок годности и условия хранения определяли согласно ОФС.1.1.0009.
Результаты и обсуждение. Получено 6 образцов гелей различного состава, содержащих исследуемую АФС МД. В каждом составе присутствовал полимер-гелеобразователь определенного происхождения (синтетический, полусинтетический или природный). Высвобождение АФС в диализную среду из разработанных лекарственных форм (ЛФ) не уступало данному параметру промышленных аналогов, а в отдельных случаях оказалось выше, чем у образцов сравнения промышленного производства. Экспериментально определены показатели стабильности и pH гелей.
Заключение. Результатом исследования является получение составов и технологии изготовления МЛФ – гелей МД с улучшенными биофармацевтическими свойствами.
Введение. В статье представлена разработка технологии получения таблеток для рассасывания методом прямого прессования с экстрактом сухим Ajania fruticulosa. Концепция Quality by Design (QbD) отражает современный подход к фармацевтической разработке, основанный на идентификации и контроле критических атрибутов качества (Critical Quality Attributes, CQA) и критических параметрах процесса (Critical Process Parameters, CPP), определяющих их вариабельность. Применение статистического планирования экспериментов (Design of Experiments, DoE) позволяет количественно оценить влияние технологических переменных и их взаимодействий, оптимизировать условия производства, снизить объем экспериментальных серий и обеспечить управляемость технологического процесса.
Цель. Разработка состава и технологии получения таблеток для рассасывания с экстрактом сухим Ajania fruticulosa методом прямого прессования с применением принципов концепции QbD и DoE.
Материалы и методы. В качестве активного фармацевтического ингредиента (АФИ) использован стандартизированный согласно Фармакопее ЕАЭС экстракт сухой Ajania fruticulosa, полученный методом мацерации с ультразвуковой интенсификацией. Таблетки для рассасывания получены методом прямого прессования с варьированием концентрации талька (0,1–3,0 %), коповидона (2,0–5,0 %) и давления прессования (15–30 кН). В качестве CQA выбраны распадаемость и истираемость. Планирование эксперимента и статистический анализ проведены с использованием программного обеспечения Minitab Statistical Software 22.3.0 (LLC "Minitab", США) с применением модуля DoE. Распадаемость и истираемость определяли в соответствии с требованиями Фармакопеи ЕАЭС на аппаратах ZT 320 и TAR 220 (ERWEKA GmbH, Германия).
Результаты и обсуждение. Оптимальная концентрация АФИ составила 1,5 %. Согласно результатам DoE, статистически значимое влияние на распадаемость оказывали содержание коповидона и давление прессования, в то время как вклад талька был незначительным. Оптимальные параметры: коповидон – 5 %, тальк – 2 %, давление прессования – 22 кН. При этих условиях распадаемость составила 12,9 мин, истираемость – 0,50 %, индекс общей желательности D = 0,8168.
Заключение. Реализация концепции QbD в сочетании с DoE обеспечила научно обоснованный подход к разработке таблеток для рассасывания с экстрактом сухим Ajania fruticulosa. Разработанные таблетки для рассасывания соответствует требованиям Фармакопеи ЕАЭС и рекомендованы для масштабирования и промышленного производства.
Введение. Контроль генерации распределения свойств гранул продукта, в частности распределения размеров, плотности и морфологии частиц, в технологии влажного гранулирования является сложным процессом, в котором одновременно происходит ряд явлений, которые в совокупности контролируют указанные фармацевтико-технологические свойства смесей. Разработанная расчетная модель процесса гранулирования позволит создавать и проектировать процессы с уменьшенным уровнем затрат, без трудоемкой экспериментальной проверки в различных масштабах работы. Понимание того, как равномерно распределить связующее вещество с помощью расчетной модели, не только поможет контролировать распределение зародышей гранул, но и приведет к более управляемому технологическому процессу. Одним из критериев устойчивой расчетной модели процесса гранулирования является уменьшение неликвидных партий продуктов, не соответствующих спецификациям.
Цель. Применение разработанной расчетной модели для оптимизации процесса гранулирования твердых лекарственных форм.
Материалы и методы. Для разработки расчетной модели процесса гранулирования были использованы и объединены формулы определения насыпной плотности до и после уплотнения, краевого угла смачивания, насыпной плотности, эффективной пористости, уравнения гидродинамики Козени – Кармана, модифицированное дифференциальное уравнение Лукаса – Уошберна, уравнения скорости распыления и движения частиц в зоне распыления, времени проникновения капли в порошковый слой и безразмерного потока распыления. Объектом исследования экспериментального подтверждения разработанной расчетной модели процесса гранулирования являлся порошок лекарственного средства, содержащий активную фармацевтическую субстанцию на основе производного 3,7-диазабицикло[3.3.1]нонана – ТСТ-9 и подлежащий дальнейшему таблетированию. В качестве увлажнителей в экспериментальных исследованиях рассматривали использование следующих жидкостей: воды очищенной и раствора гипромеллозы. Вязкость образцов измерялась с помощью вибровискозиметра SV-10 (A&D, Япония). Экспериментальное гранулирование проводилось в установке с псевдоожиженным слоем. Для определения показателей качества смеси и гранул использовались тестер сыпучести ручной с цифровым измерителем высоты EFT-01 (Electrolab, Индия) и тестер насыпной плотности ETD-1020 (Electrolab, Индия). Поверхностное натяжение гранулирующих жидкостей измерялось на тензиометре К6 по методу отрыва кольца (метод дю Нуи) (KRÜSS GmbH, Германия).
Результаты и обсуждение. Впервые представлен алгоритм вычисления параметров расчетной модели процесса гранулирования, времени проникновения капли, которое контролируется фармацевтико-технологическими характеристиками состава лекарственной формы, и безразмерного потока распыления, который регулируется параметрами процесса. Их установленные значения позволили осуществить прогноз поведения гранул и выход продукта.
Заключение. В данной работе продемонстрировано применение расчетной модели для прогнозируемого получения гранул на примере разработки технологии получения лекарственного средства на основе активной фармацевтической субстанции, являющейся производным 3,7-диазабицикло[3.3.1]нонана – ТСТ-9. В результате проектируемые значения расчетной модели имели подтверждение в экспериментальных исследованиях гранулирования в установке с псевдоожиженным слоем с применением различных увлажняющих жидкостей.
МЕТОДЫ АНАЛИЗА ЛЕКАРСТВЕННЫХ СРЕДСТВ
Введение. Синюха голубая является единственным представителем семейства синюховых, который допустим к использованию в медицинской практике. Синюхи голубой корневища с корнями применяются в качестве отхаркивающего и седативного средства и включены в Государственную фармакопею XIV изд. Трава растения используется в качестве биологически активной добавки седативного действия, однако нормативная документация на данный вид сырья до настоящего времени не разработана.
Цель. Описание анатомических признаков, необходимых при разработке проекта фармакопейной статьи для формирования раздела «Микроскопия» и оценки подлинности растительного сырья «Синюхи голубой трава».
Материалы и методы. В работе использовались несколько образцов синюхи голубой травы, которые были собраны самостоятельно от культивируемых растений (Polemonium cаeruleum L.) в 2022 и 2023 гг. в период массового цветения на территории Ботанического сада им. Б. М. Козо-Полянского ФГБОУ ВО ВГУ (Воронеж). Микроскопический анализ выполняли в соответствии с требованиями действующей нормативной документации.
Результаты и обсуждение. Установлено, что эпидермальные клетки листа, чашечки и венчика синюхи голубой извилистые, на цветоносах – вытянутые. Трихомы двух типов. По краю листа и на чашелистиках находятся сосочковидные выросты эпидермиса. Мезофилл снизу листа представлен губчатой тканью. Проводящая система преимущественно спирального типа утолщения. Устьица аномоцитного типа. Стебель округлый или со слабо выраженными гранями. Первичная кора стебля представлена колленхимой, запасающей паренхимой без включений, эндодермой с поясками Каспари. Стела беспучкового строения. Камбий состоит из сплошных рядов мелких клеток. Флоэма представлена мелкими клетками. Во вторичной ксилеме отсутствуют сердцевидные лучи, радиально расположенные сосуды имеют толстые стенки. Сердцевина представлена клетками паренхимы с каплями масла. Черешок в очертании треугольный, с глубокой выемкой сверху и длинными краевыми выростами, где находится по одному мелкому проводящему пучку. Центральный пучок в форме дуги с загнутыми вовнутрь краями с паренхимной обкладкой.
Заключение. В рамках настоящего исследования с помощью различных приемов микроскопического анализа изучены анатомо-диагностические признаки синюхи голубой травы. Полученные данные будут использованы при разработке проекта фармакопейной статьи «Синюхи голубой трава», а именно для формирования раздела «Микроскопия».
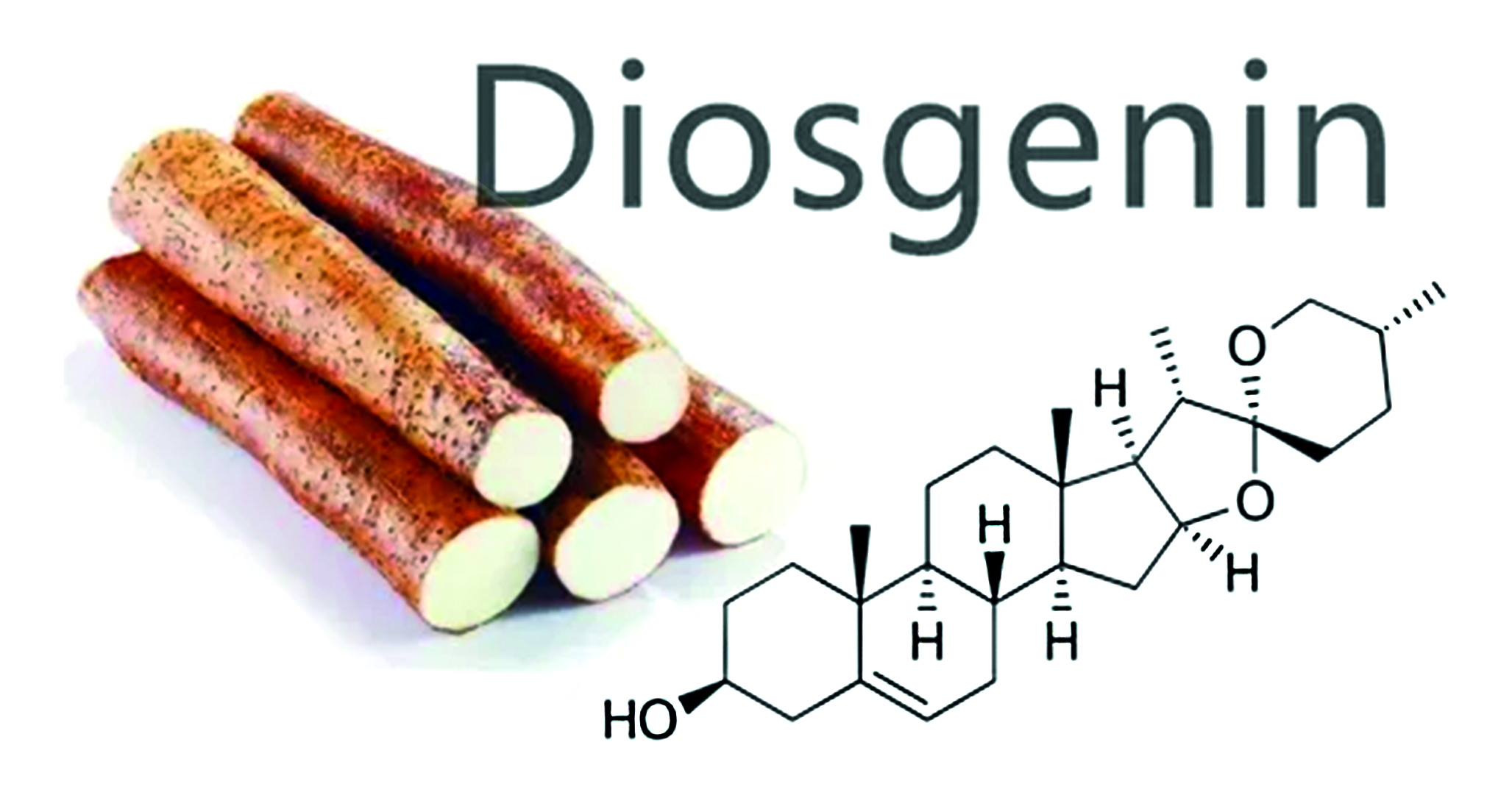
Введение. В оригинальной статье представлены результаты экспериментального исследования, проведенного с использованием метода высокоэффективной тонкослойной хроматографии (ВЭТСХ), растительных образцов – корневищ с корнями Dioscorea caucasica Lipsky, Dioscorea nipponika Makino. Данные виды диоскорей используются в различных областях медицины в качестве фунгицидного, антимикробного, а также антисклеротического средства. Метод ВЭТСХ используется на этапе скрининга растительных образцов для предварительной идентификации и денситометрического количественного определения диосгенина в растительных экстрактах.
Цель. Разработка ВЭТСХ-методики количественной оценки содержания диосгенина после проведения кислотного гидролиза экстрактов в воздушно-сухом сырье – корневищах с корнями Dioscorea caucasica Lipsky, Dioscorea nipponika Makino.
Материалы и методы. Экстракты получали путем предварительного обезжиривания и депигментирования воздушно-сухого сырья корневищ с корнями изучаемых видов диоскорей дихлорметаном х.ч. с последующим двойным экстрагированием. Первое экстрагирование проводили в среде 50%-го водного раствора изопропанола х.ч. при озвучивании ультразвуком с последующим проведением кислотного гидролиза О-гликозидных связей, упариванием. Второе экстрагирование проводили путем перерастворения сухого остатка в метаноле х.ч.; очищали от взвешенных частиц фильтрованием через шприцевые фильтры с диаметром перфораций 20 мкм. ВЭТСХ осуществляли на аппаратном комплексе CAMAG (Швейцария) с использованием пластин HPTLC Aluminium sheets Silica gel 60 F254, 20 × 20 см, которые разрезали до размера 20 × 10 см.
Результаты и обсуждение. После проведения сканирующей денситометрии при 366 и 542 нм было установлено, что хроматографирование метанольных извлечений в системе растворителей толуол х.ч. – хлороформ х.ч. – ацетон х.ч. (2 : 8 : 2 по объему) позволяет удовлетворительно провести разделение и последующее денситометрическое количественное определение диосгенина. Сравнение треков растительных экстрактов корневищ с корнями Dioscorea caucasica Lipsky и Dioscorea nipponika Makino проводили со стандартным образцом диосгенина.
Заключение. Проведенное исследование позволило установить, что содержание стероидного сапогенина диосгенина в воздушно-сухом сырье Dioscorea nipponica Makino (286,4–296,3 мкг/г) незначительно преобладает над его содержанием в сырье Dioscorea caucasica Lipsky (257–277,1 мкг/г). Полученные количественные значения, рассчитанные раздельно по высоте и площади пиков, демонстрируют хорошую сходимость, что подтверждает корректность методики. Разработанный метод высокоэффективной тонкослойной хроматографии с денситометрическим детектированием диосгенина может быть рекомендован для рутинного количественного анализа данного соединения в растительном сырье.
Введение. Около 30 % генно-инженерных терапевтических белков производится в Escherichia coli. При наработке рекомбинантных белков одним из факторов, определяющих эффективность процесса и качество продукта, является показатель жизнеспособности клеток. Важно контролировать жизнеспособность при формировании банков клеток и оценке их стабильности в процессе хранения, а также при разработке условий культивирования штаммов. Изменение условий хранения или культивирования может приводить к изменению структуры клеточной популяции с изменением соотношения жизнеспособных, мертвых и находящихся в апоптозоподобной гибели (ALD, apoptosis-like death) клеток. Одним из способов оценки популяций клеток может являться метод проточной цитометрии с окрашиванием.
Цель. Разработать, валидировать и апробировать методику оценки жизнеспособности E. coli с использованием проточной цитометрии.
Материалы и методы. Для оценки жизнеспособности клеток проводили окрашивание E. coli пропидия йодидом (PI) и аннексином V-FITC (An-V-FITC). При помощи двойного окрашивания определяли популяции клеток живых, мертвых и в ALD. Валидацию методики проводили согласно Государственной фармакопее, решению Совета ЕЭК № 85 от 03.11.2016 и рекомендациям ICH. Анализировали применимость методики при разработке условий создания банков клеток и их культивировании.
Результаты и обсуждение. Разработана методика оценки жизнеспособности E. coli с использованием проточной цитометрии и окрашивания PI с An-V-FITC, позволяющая оценить популяции клеток живых, мертвых и в ALD. По итогам валидации методики установлено ее соответствие критериям: специфичности (6 %), линейности (R2 > 0,9), правильности (97–102 %), пределу количественного определения (подтвержден, 117 %), сходимости (1–10 %), внутрилабораторной прецизионности (2–17 %), аналитической области (6,4–100 %). При оптимизации условий создания банков клеток оценка жизнеспособности позволила определить, что для получения более 97 % жизнеспособных клеток после выхода из криоконсервации необходимо использовать соотношение объемов культуральной жидкости и криопротектора 3 к 1 при оптической плотности суспензии OD600 = 15. При разработке процесса культивирования штамма методика позволила определить оптимальные условия, в результате в биореакторе за 8 часов индукции процент мертвых клеток увеличился всего на 2,5 %, а клеток в состоянии ALD – на 7 %.
Заключение. Разработана и валидирована методика для оценки жизнеспособности E. coli, она может использоваться на этапе разработки и производства терапевтических продуктов.
Введение. Флоротанины, являющиеся вторичными метаболитами, в основном вырабатываются бурыми морскими водорослями и относятся к классу полифенольных соединений, обладающих разнообразной биологической активностью. Бурые водоросли, выбрасываемые на берег штормом и составляющие угрозу для прибрежных экосистем, могут стать ценным источником полифенолов. Для количественного определения общего содержания полифенолов в природных образцах чаще всего применяется реактив Фолина – Чокальтеу (FCR).
Цель. Основной целью данного исследования является стандартизация и валидация спектрофотометрического определения общего содержания флоротаннинов с использованием FCR и демонстрация его применимости для анализа выброшенных штормом и свежих водорослей.
Материалы и методы. Образцы A. nodosum были собраны на защищенном пляже губы Оленица (66°27'15.7" с.ш. 35°18'20.4" в.д.) Кандалакшского залива (Белое море, Россия) на двух приливных уровнях: один находился во время отлива на глубине 0,6–1,0 м (свежие водоросли), а второй – на супралиторали в зоне заплеска волн (водоросли из штормовых выбросов). Полевой отбор проб проводился в период с июня по сентябрь. Очищенные водоросли доставляли в лабораторию, тщательно промывали чистой водой, лиофильно высушивали и измельчались в порошок. Функциональные группы, присутствующие в водорослях, идентифицировались с помощью инфракрасной Фурье-спектроскопии (ИК-Фурье). Спектрофотометрический метод с использованием реактива Фолина – Чокальтеу оптимизирован для анализа свежих и выброшенных штормом бурых водорослей и валидирован в соответствии с национальными и международными рекомендациями.
Результаты и обсуждение. Оптимальными условиями для анализа были время анализа, длина волны и стандартное вещество: 45 мин, 750 нм и флороглюцин, соответственно. В этих условиях валидация методики спектрофотометрии показала, что метод линейный (R2 > 0,99), специфичный, точный, достоверный, воспроизводимый, надежный и простой в применении. Предел обнаружения и предел количественного определения составили 0,005 и 0,02 мг/мл, соответственно. Внутридневная (RSD 2,16 %) и междневная (RSD 2,84 %) прецизионность анализа была рассчитана. Оценка влияния матрицы показала, что она оказывает незначительное влияние (1,9 %) на количественное определение флоротаннинов. Содержание флоротаннинов в водорослях, выброшенных штормом, варьировалось от 59 до 101 мг/г, в то время как в свежесобранных водорослях было статистически достоверно выше (р < 0.01) и варьировалось от 71 до 135 мг/г. Максимальное накопление флоротаннинов в A. nodosum наблюдалось в период с июля по август, после чего наблюдалось снижение.
Заключение. Полученные в ходе данного исследования результаты могут быть применены для регулярного анализа содержания флоротаннинов в бурых водорослях и водорослях, извлеченных из штормовых отходов. Это возможно благодаря оптимизированному спектрофотометрическому методу с использованием реактива Фолина – Чокальтеу, который основывается на применении доступного и недорогого оборудования, имеющегося в большинстве лабораторий, что обеспечивает оперативность анализа. Данная методология соответствует требованиям фармацевтического анализа, обеспечивая надежность результатов при разработке лекарственных препаратов и рутинном контроле как свежего, так и штормовых выбросов A. nodosum.
Введение. В результате поиска более активных в отношении рака простаты полифторсодержащих структурных аналогов нестероидного антиандрогена флутамида был получен ряд соединений, среди которых наибольший интерес для дальнейшего изучения представлял 2,2,3,3,4,4,5,5,6,6,7,7,8,8,9,9,9-гептадекафтор-N-(4-нитро-3-(трифторметил)фенил) нонанамид (шифр F-4). Необходимые данные для строгого доказательства строения молекулы данного соединения ранее получены не были. Идентификация примесей и количественная оценка их содержания в субстанции F-4 не проводились. Для решения этих задач нами были использованы методы спектроскопии ядерного магнитного резонанса (ЯМР) и высокоэффективной жидкостной хроматографии с ультрафиолетовым (ВЭЖХ-УФ) и тандемным масс-селективным детектированием (ВЭЖХ-МС/МС).
Цель. Комплексный анализ строения соединения F-4 методами ЯМР и ВЭЖХ, а также идентификация и количественная оценка с их помощью содержания примесей в образцах субстанции.
Материалы и методы. Объектом исследования являлись лабораторные образцы субстанции соединения F-4, полученные ацилированием 4-нитро-3-(трифторметил)анилина хлорангидридом перфторпеларгоновой кислоты известным методом. Для анализа использовали: ЯМР-спектрометр Agilent DD2 NMR System 600; жидкостный хроматограф Agilent 1200, оснащенный диодно-матричным детектором G1315B; жидкостный хроматограф Agilent Infinity II, снабженный масс-спектрометрическим детектором с тройным квадруполем G6495C (Agilent Technologies, США). В обоих хроматографах применялась колонка Luna C18(2), 250 × 4,6 мм, 5 мкм (Phenomenex, США).
Результаты и обсуждение. Структурная интерпретация спектров 1Н-, 13С- и 19F-ЯМР образцов соединения F-4, проведенная с учетом значений химических сдвигов сигналов, их мультиплетности и данных 2D-экспериментов, однозначно свидетельствует о том, что F-4 имеет структуру 2,2,3,3,4,4,5,5,6,6,7,7,8,8,9,9,9-гептадекафтор-N-(4-нитро-3-(трифторметил) фенил)нонанамида. В спектрах 1Н- и 19F-ЯМР образцов субстанции F-4 также присутствовали сигналы двух примесных соединений, не относящихся к исходным веществам. Для их разделения был использован метод ВЭЖХ-УФ. С помощью ВЭЖХ-МС/МС при ионизации электроспреем в отрицательном режиме (–ESI) для всех пиков были зафиксированы высокоинтенсивные сигналы m/z, характерные для депротонированных молекулярных ионов. Строение обнаруженных примесей было подтверждено методами спектроскопии ЯМР. Результаты количественного определения относительного содержания примесей в образцах субстанции F-4 с применением методов 1Н- и 19F-ЯМР практически совпали, различия между полученными средними значениями статистически не были значимы.
Заключение. В результате комплексного исследования методами ЯМР и ВЭЖХ установлено, что соединение F-4 соответствует структуре 2,2,3,3,4,4,5,5,6,6,7,7,8,8,9,9,9-гептадекафтор-N-(4-нитро-3-(трифторметил)фенил)нонанамида. В образцах субстанции F-4 были идентифицированы две родственные примеси, относительное содержание каждой примеси не превышало 1,7 %.
Введение. Венозные тромбоэмболии и фибрилляция предсердий являются значимыми причинами сосудистой смертности. Антикоагулянтная терапия существенно снижает риск ишемического инсульта, а дабигатрана этексилат, относящийся к прямым ингибиторам тромбина, прочно вошел в клиническую практику. На российском рынке представлены воспроизведенные препараты дабигатрана этексилата в форме капсул, одним из наиболее критичных видов контроля качества для данной лекарственной формы является тест сравнительной кинетики растворения (ТСКР). Использование биорелевантных сред для растворения позволяет достоверно прогнозировать поведение капсул in vivo. Для проведения ТСКР капсул дабигатрана этексилата исходя из фармакокинетических свойств наиболее подходящей средой является Fasted State Simulated Gastric Fluid (FaSSGF).
Цель. Разработка и валидация аналитических методик количественного определения дабигатрана этексилата методами высокоэффективной жидкостной хроматографии с диодно-матричным детектированием (ВЭЖХ-ДМД) и спектрофотометрии в ультрафиолетовой области (УФ-спектрофотометрия) при проведении ТСКР капсул, содержащих дабигатрана этексилат, в биорелевантной среде растворения FaSSGF.
Материалы и методы. Анализировали модельные растворы, содержащие пеллеты дабигатрана этексилата и вспомогательные вещества лекарственного препарата. Для хроматографического разделения использовали ВЭЖХ-ДМД Agilent 1260 Infinity II Series (США). Детектирование проводилось при длине волны 316 нм. Использовали колонку ZORBAX SB-C18, 150 × 4,6 мм, 5 мкм, предколонку ZORBAX SB-C18, 12,5 × 4,6 мм, 5 мкм (Agilent Technologies, США). Для разработки и валидации метода УФ-спектрофотометрии использовали спектрофотометр СФ-2000 (Россия). Обработку первичных данных проводили с помощью программного обеспечения Open Lab CDS v. 2.7 для ВЭЖХ, «Сканирование для спектрофотометра СФ-2000» от ООО «ОКБ Спектр», версия 4.06.
Результаты и обсуждение. Подобраны оптимальные условия пробоподготовки, хроматографические и спектрофотометрические условия для количественной оценки дабигатрана этексилата, высвобождаемого в среду растворения FaSSGF, проведена валидация разработанных аналитических методик в диапазоне от 0,13 до 14,67 мкг/мл.
Заключение. Аналитические методики обеспечивают воспроизводимые и достоверные результаты во всем заданном диапазоне и пригодны для количественного определения дабигатрана этексилата при проведении ТСКР в биорелевантной среде растворения FaSSGF.
Введение. Листья облепихи крушиновидной в настоящее время используются в фармации в качестве исходного сырья для производства лекарственного растительного препарата (ЛРП) «Гипорамин» противовирусного действия. В научной литературе представлены данные доклинических испытаний экстрактов из листьев, подтверждающие их противовоспалительную, антибактериальную, антиоксидантную, иммуномодулирующую активность, а также имеются данные о потенциальных свойствах гепатопротектора, что связано с фенольной, в том числе флавоноидной, фракцией листьев. Поэтому исследования возможности дополнительных путей внедрения изучаемого сырья в практическую фармацию, а также расширения ассортимента отечественных ЛРП, содержащих комплекс биологически активных веществ (БАВ) листьев, например в виде настоек и жидких экстрактов на основе листьев, с разработкой методик их стандартизации по целевой группе БАВ следует считать актуальными.
Цель. Целью исследования являлось получение и стандартизация водно-спиртовых извлечений из облепихи крушиновидной листьев.
Материалы и методы. Сравнительное исследование проводили для извлечений из высушенных листьев, приготовленных по типу настоек (1 : 5), полученных различными способами, и экстракта жидкого (1 : 1) по стандартным фармакопейным методикам. Все исследуемые извлечения готовили из листьев, заготовленных в 2024 году на территории Воронежской области, фенологической фазы развития, соответствующей стадии технической зрелости плодов. Проводилась разработка методик идентификации и количественного определения флавоноидов методами ТСХ и дифференциальной спектрофотометрии.
Результаты и обсуждение. По показателю «сухой остаток» наибольшее количество экстрактивных веществ показала настойка, полученная методом дробной мацерации. Жидкий экстракт демонстрировал самый высокий выход БАВ. Содержание тяжелых металлов не превышало нормативов, рекомендованных Государственной фармакопеей РФ. Содержание флавоноидов максимально было в экстракте жидком (1 : 1). С точки зрения эффективности использования сырья наилучшей формой является настойка, полученная методом перколяции.
Заключение. Получены опытные лабораторные образцы жидких водно-спиртовых ЛФ на основе листьев облепихи крушиновидной (настойки, экстракт жидкий), проведена их стандартизация по показателям, изложенным в нормативной документации, разработаны методики количественного определения флавоноидов. Методом ТСХ показан неодинаковый флавоноидный состав водно-спиртовых извлечений, в которые переходит от 11 до 18 БАВ группы флавоноидов. Наиболее высокое содержание флавоноидов отмечено для экстракта жидкого (1 : 1), что позволяет рекомендовать данную форму в качестве оптимальной из исследованных.
Введение. Плоды фенхеля обладают выраженной ветрогонной и спазмолитической активностью благодаря особенности состава эфирного масла, доминирующим компонентом которого является фенилпропаноид – транс-анетол. Его содержание в эфирном масле может варьироваться в широком диапазоне. При этом в Российской фармакопее XV издания стандартизация по содержанию анетола для плодов фенхеля не предусмотрена.
Цель. Разработка и валидационная оценка спектрофотометрической методики определения суммы ароматических соединений в пересчете на анетол в эфирном масле плодов фенхеля обыкновенного.
Материал и методы. В качестве объекта исследования использовались плоды фенхеля обыкновенного (Foeniculum vulgare Mill.) производства ООО Фирма «Здоровье» 2024 года. В работе использовали спектрофотометр UNICO-2802 (Россия), весы аналитические АДВ-200М (Россия), газовый хроматограф GCMS-QP2010 Ultra (Shimadzu, Япония), совмещенный с масс-селективным детектором. При спектрофотометрическом определении навески эфирного масла и стандартного образца анетола растворяли в 95%-м спирте и снимали оптические плотности растворов при длине волны 259 нм в кюветах с толщиной слоя 10 мм. Результаты спектрофотометрической методики подтверждали с помощью газовой хроматографии.
Результаты и обсуждение. Валидация представленной методики, проведенная в соответствии с требованиями ОФС.1.1.0012 «Валидация аналитических методик» Государственной фармакопеи XV издания, показала ее специфичность, линейность, прецизионность и правильность. Результаты не отягощены систематической погрешностью. Относительное стандартное отклонение (RSD) не превышает 2,0 %. Результаты спектрофотометрического определения суммы ароматических соединений в пересчете на анетол (46,5 ± 0,7 %) коррелируют с результатами ГЖХ-анализа (48,6 ± 1,1 %).
Заключение. Разработанная методика количественного определения суммы ароматических соединений в пересчете на анетол может быть использована для стандартизации как самих плодов фенхеля обыкновенного путем введения дополнительного критерия оценки качества его эфирного масла в раздел «Количественное определение», так и эфирного масла фенхеля, используемого в качестве субстанции для изготовления лекарственных препаратов.
ДОКЛИНИЧЕСКИЕ И КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Введение. Нарушения в функционировании ЦНС, возникающие при хроническом употреблении этанола, часто связаны с угнетением полноценного нейрогенеза. При этом одними из ведущих сигнальных каскадов, задействованных в регуляции пролиферации и дифференцировки нейральных и нейрональных стволовых клеток, считаются GPCR/cAMP-зависимый путь и JAK/STAT-сигналинг. Очевидно, что поиск принципиально новых подходов к терапии этаноловой нейродегенерации, путем воздействия на внутриклеточные сигнальные молекулы, весьма актуален и востребован для практической медицины.
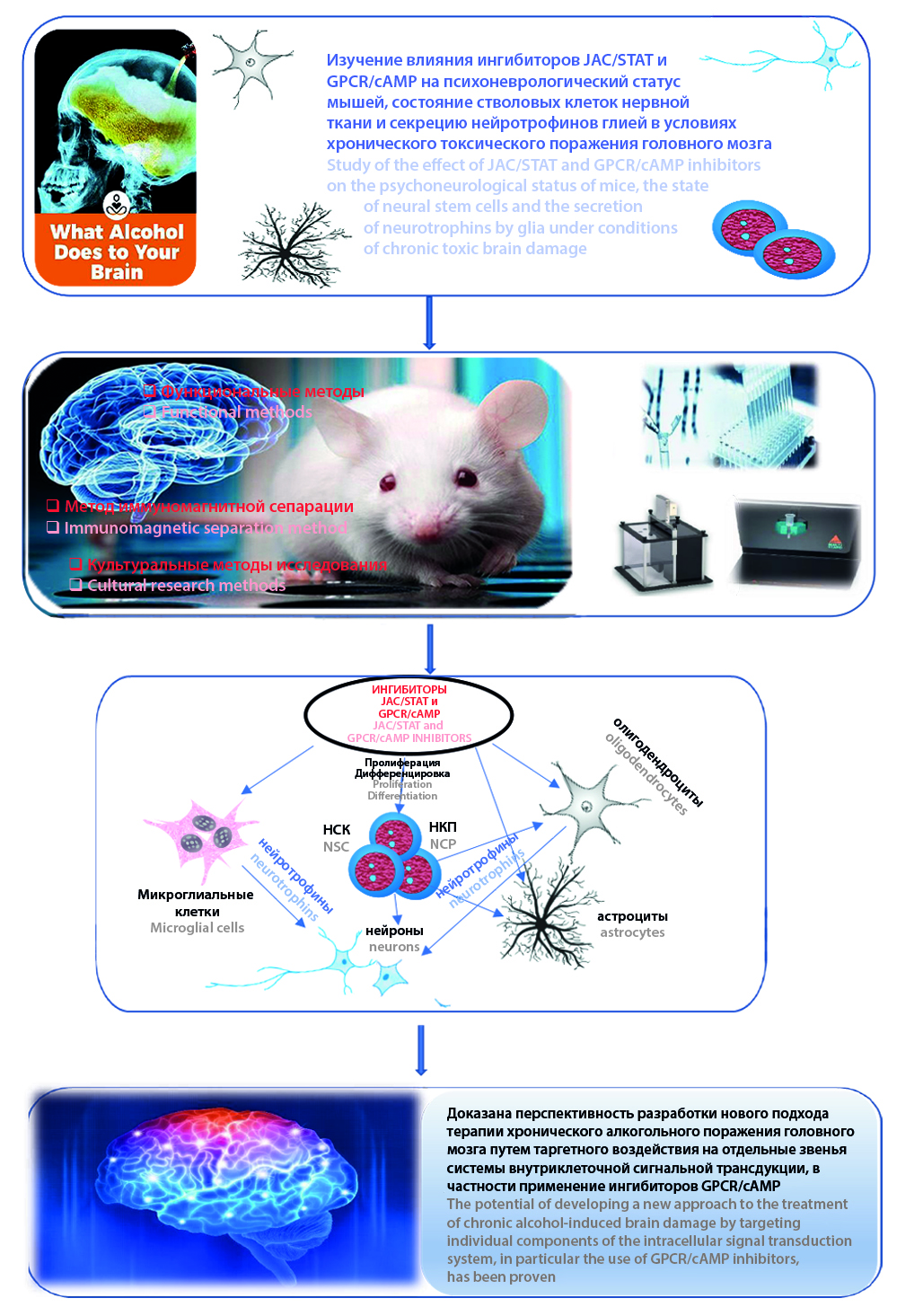
Цель. Целью данного исследования явилось изучение влияния ингибиторов JAC/STAT и GPCR/cAMP на психоневрологический статус мышей, состояние стволовых клеток нервной ткани и секрецию нейротрофинов глией в условиях хронического токсического поражения головного мозга.
Материал и методы. Исследования проведены на 90 мышах линии С57BL/6. Алкогольную нейродегенерацию моделировали введением per os 30%-го раствора С2Н5ОН в дозе 3 г/кг/сут в течение 8 недель. Ингибиторы JAC/STAT и GPCR/cAMP вводили подкожно 1 раз в сутки в течение 7 дней в дозе 15 и 10 мкг/кг соответственно. Психофармакологические эффекты блокаторов оценивали в тесте «Открытое поле» и по степени сохранности условного рефлекса пассивного избегания. Культуральными методами изучали содержание нейральных стволовых клеток и коммитированных нейрональных предшественников в субвентрикулярной зоне головного мозга, их пролиферативную активность и интенсивность созревания, исследовали продукцию нейротрофных факторов клетками глии.
Результаты и обсуждение. Введение ингибиторов JAC/STAT и GPCR/cAMP корригировало функциональные признаки патологии мозга алкогольного генеза (наблюдалась отмена изменений ориентировочно-исследовательского поведения). При этом курсовое применение ингибитора GPCR/cAMP нивелировало, а введение блокатора JAC/STAT усугубляло снижение уровня воспроизведения условного рефлекса пассивного избегания у алкоголизированных мышей. В группах животных, получавших ингибиторы JAC/STAT и GPCR/cAMP, отмечалось возрастание числа нейральных стволовых клеток и коммитированных нейрональных предшественников, сопровождающееся повышением их митотической активности и интенсивности специализации. Введение ингибитора GPCR/cAMP после моделирования этанолиндуцированного поражения головного мозга сопровождалось повышением секреции нейротрофинов астроцитами и микроглией.
Заключение. Полученные результаты указывают на перспективность разработки нового подхода к терапии хронического алкогольного поражения головного мозга путем таргетного воздействия на отдельные звенья системы внутриклеточной сигнальной трансдукции, в частности применение ингибиторов GPCR/cAMP.
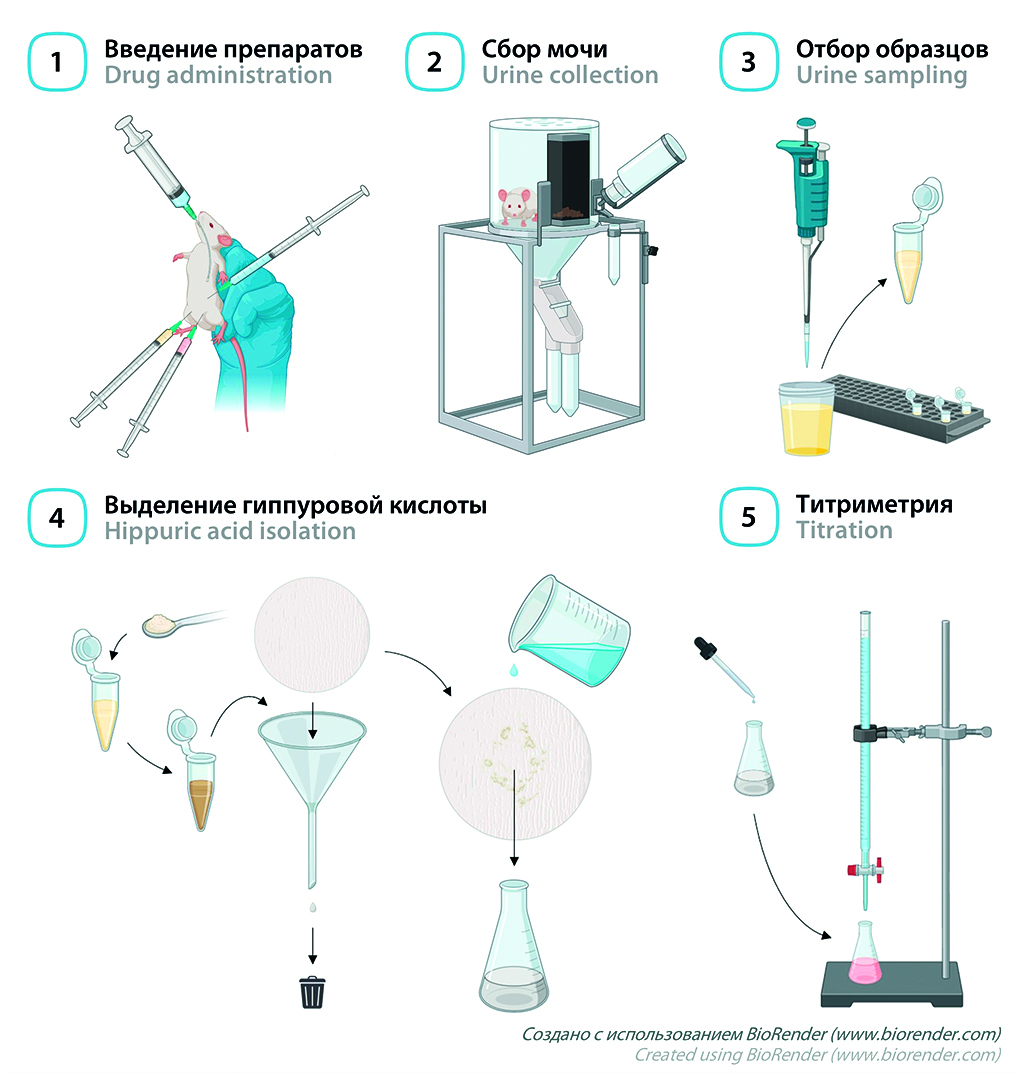
Введение. Функциональные печеночные пробы являются актуальной группой методик скрининговой оценки состояния печени, применимых как в лабораторных исследованиях, так и в клинической практике. В эту группу в том числе входит проба Квика – Пытеля, основанная на ферментативной реакции образования гиппуровой кислоты из глицина и бензоата в печени. Эта проба отличается малой инвазивностью и сравнительной простотой выполнения, однако в настоящий момент отсутствует детализированный протокол ее проведения у мелких лабораторных животных.
Цель. Целью работы являлась адаптация протокола пробы Квика – Пытеля для оценки антитоксической функции печени у мышей.
Материалы и методы. Белым беспородным мышам-самцам (n = 10) вводили внутрибрюшинно нагрузочные дозы натрия бензоата и глицина в эквимолярном соотношении (504 мг/кг и 264 мг/кг соответственно), после чего в течение 18 ч собирали мочу в метаболических клетках. После пробоподготовки титровали образовавшуюся гиппуровую кислоту 0,01 Н раствором калия гидроксида в присутствии 1%-го раствора фенолфталеина. Через 1 неделю после измерения мышам вводили тетрахлорметан (1 мл/кг) для индукции острого токсического гепатита, после чего проводили пробу повторно. Поражение печени верифицировали гистологически с окрашиванием гематоксилином и эозином.
Результаты и обсуждение. После введения тетрахлорметана концентрация гиппуровой кислоты в моче статистически значимо (p < 0,01) снизилась более чем на 50 % от исходного уровня. В образцах печени при этом наблюдали характерную морфологическую картину острого токсического гепатита.
Заключение. Проведена адаптация протокола пробы Квика – Пытеля для мышей и подтверждена ее применимость для оценки антитоксической функции печени при остром поражении. Описанная в работе методика проста в исполнении, не требует существенных затрат и может быть использована для рутинной оценки функционального состояния печени у мелких лабораторных животных.
Введение. Пациенты с диагнозом туберкулеза легких с множественной (МЛУ-ТБ) или широкой лекарственной устойчивостью возбудителя (ШЛУ-ТБ) отличаются сниженной массой тела, что при стандартном режиме дозирования противотуберкулезных препаратов может приводить к изменению фармакокинетических параметров лекарственных средств, увеличивая риск возникновения нежелательных побочных реакций или снижения терапевтической эффективности. В связи с этим актуальной задачей является математическое моделирование влияния массы тела на фармакокинетику нового отечественного препарата тиозонид для обоснования оптимальных режимов дозирования.
Цель. Разработка математической модели влияния массы тела на фармакокинетические показатели препарата тиозонид и моделирование влияния массы тела пациентов на режим дозирования.
Материалы и методы. Для моделирования использовалась программная среда Julia и пакет Pumas.jl. Разработана двухкомпартментная фармакокинетическая модель с кинетикой первого порядка и абсорбцией, модифицированной при помощи функции Вейбулла. Для каждого сценария были взяты группы пациентов с различной фиксированной массой тела (40, 50, 60, 70 и 80 кг) и было выполнено 10 000 симуляций.
Результаты и обсуждение. Анализ результатов симуляций показал, что максимальная концентрация препарата (Cmax) увеличивается при снижении массы тела, однако максимальное относительное различие между крайними группами (40 и 80 кг) составило 17,08 %. Минимальные концентрации (Ctau) были стабильны во всех группах, демонстрируя относительные изменения менее 2,5 %. Площадь под кривой «концентрация – время» (AUCtau) варьировалась от 2,88 до 7,23 %.
Заключение. Разработана математическая модель влияния массы тела на фармакокинетические параметры нового отечественного препарата тиозонид. Проведенное исследование установило отсутствие необходимости изменения режима дозирования тиозонида у пациентов с массой тела от 40 до 80 кг.
Введение. Одним из актуальных направлений современной фармации является создание высокоэффективных и безопасных лекарственных средств. Поиск противоопухолевых средств в связи с ростом онкологических заболеваний направлен на получение таргетных препаратов. Синтезированные в Пермской государственной фармацевтической академии производные 2-аминопиррола продемонстрировали высокую цитостатическую активность, обусловленную активизацией механизма апоптоза опухолевых клеток в М-фазе. В объеме доклинических исследований необходимо оценить острую токсичность и определить фармакокинетические параметры наиболее активного соединения 2-AНПК.
Цель. Изучение острой токсичности в опытах на мышах и крысах и фармакокинетических параметров 2-AНПК после однократного введения крысам линии Wistar.
Материалы и методы. Оценка острой токсичности при пероральном введении с вычислением LD50 методом пробит-анализа данных Finney проведена в опытах на белых нелинейных мышах и крысах линии Wistar. Фармакокинетические параметры 2-AНПК исследованы на крысах-самцах линии Wistar после введения соединения per os. Для количественного определения 2-AНПК в плазме крови животных использована валидированная методика на основе высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием (ВЭЖХ-МС/МС).
Результаты и обсуждение. LD50 соединения при однократном пероральном введении определена на уровне 4434 мг/кг для мышей и 1547 мг/кг для крыс. Время достижения максимальной концентрации 2-AНПК в организме крыс при однократном введении 150 мг/кг составляет 2,90 ± 0,32 ч, период полувыведения соединения из организма – 4,50 ± 0,49 ч. Расчетная величина кажущегося объема распределения, значительно превышающая анатомический объем, указывает на преимущественное локализацию вещества во внесосудистом пространстве.
Заключение. В ходе изучения острой токсичности на мышах установлено, что 2-AНПК относится к 4 классу токсичности (малотоксичные) по классификации Hodge и Sterner и 5 классу опасности химической продукции по воздействию на организм. В эксперименте на крысах проведена оценка фармакокинетических параметров 2-AНПК после перорального введения. Полученные данные показывают потенциальную возможность создания на основе нового производного 2-аминопиррола с доказанной противоопухолевой активностью лекарственной формы для перорального применения.
Введение. Гепатотоксичность циклофосфамида в первую очередь обусловлена влиянием его метаболитов, в том числе акролеина. Антиоксидантные свойства были продемонстрированы дапаглифлозином (Dapa), ингибитором натрий-глюкозного котранспортера-2 (SGLT2). Силимарин (Sil) – это химическое вещество, извлекаемое из расторопши пятнистой. Исследования показали, что силимарин обладает гепатопротекторными и антиоксидантными свойствами.
Цель. Целью данного исследования было сравнение гепатопротекторных эффектов дапаглифлозина и силимарина на модели поражения печени, вызванного ЦФД, у крыс.
Материалы и методы. В качестве отрицательного контроля использовались: растворитель (2%-й водный раствор карбоксиметилцеллюлозы натрия, КМЦ), циклофосфамид (30 мг/кг/день, внутрибрюшинно), дапаглифлозин + циклофосфамид (3 мг/кг/день, перорально) и силимарин + циклофосфамид (200 мг/кг/день, перорально). 50 крыс были случайно распределены на 5 групп по 10 животных в каждой. Через десять дней оценивали уровни аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке крови; в тканях печени измеряли уровни малонового диальдегида (MDA), восстановленного глутатиона (GSH) и супероксиддисмутазы (СОД); также проводили гистологическое исследование образцов.
Результаты и обсуждение. Уровни ALT, AST и MDA значительно повышались под действием циклофосфамида, в то время как уровни GSH и СОД снижались (P < 0,05). Лечение дапаглифлозином или силимарином на фоне применения ЦФД привело к значительному улучшению этих изменений (P < 0,05 по сравнению с контрольной группой). Результаты исследования показывают, что Dapa был более эффективен, чем Sil, в снижении уровня MDA и повышении уровня GSH и SOD (P < 0,05). В группе Dapa (группа IV) гистологическое исследование показало, что строение печени осталось неизменным, и наблюдалось лишь незначительное увеличение сосудистого застоя.
Заключение. И дапаглифлозин, и силимарин оказывают сопоставимое гепатопротекторное действие против вызванного циклофосфамидом поражения печени, возможно, за счет ослабления окислительного стресса и сохранения целостности гепатоцитов. Данное исследование дополняет имеющиеся данные, подтверждающие использование каждого из этих препаратов в моделях поражения печени. Однако, в отличие от исследования Сатьяма и др. (2024), в котором изучалось их комбинированное действие, данное исследование подчеркивает их индивидуальную эффективность в модели токсичности, специфичной для циклофосфамида.
ЮБИЛЕЙ
НЕКРОЛОГ
ИСПРАВЛЕНИЯ
Разработка и регистрация лекарственных средств. 2025;14(2):54–74. https://doi.org/10.33380/2305-2066-2025-14-2-2084. Статья опубликована: 20.05.2025.
Разработка и регистрация лекарственных средств. 2025;14(4):101–107. https://doi.org/10.33380/2305-2066-2025-14-4-2195. Статья опубликована: 24.10.2025.
Новости отрасли
2026-04-13
Регистрация на XV Международный фармацевтический форум ФармПРО-2026
 | 23 апреля 2026 года в Москве, в отеле «Сафмар Грандъ Москва», состоится XV Международный фармацевтический форум ФармПРО-2026 – одно из ключевых отраслевых событий для руководителей и экспертов фармацевтической индустрии. |
2026-04-13
Международный форум "Биопром: промышленность и технологии для человека" пройдет в Геленджике 5-6 октября 2026 года
 | Приглашаем вас на международный форум БИОПРОМ: промышленность и технологии для человека — платформу сотрудничества ключевых производителей и институтов, работающих над созданием технологий для улучшения качества жизни человека. |
2026-04-07
Двухдневный XIX конгресс «Разработка и регистрация лекарственных средств» прошел 17 и 18 февраля 2026 года в конгресс-центре Сеченовского университета в Москве.
 | Организаторами конгресса выступают Центр Фармацевтической Аналитики, журнал «Разработка и регистрация лекарственных средств», журнал «Гербариум» и Санкт-Петербургский государственный химико-фармацевтический университет. Мероприятие посетили порядка 200+ слушателей, с нами были более 95 докладчиков, нас поддержали 20+ партнеров. |
| Ещё новости |
ISSN 2658-5049 (Online)