ОТ РЕДАКЦИИ
Конгресс "Химико-фармацевтические и биологические препараты: фармацевтическая и клиническая разработка согласно правилам ЕАЭС" пройдет в Москве 22 сентября. Мероприятие посвящено обсуждению таких важных тем, как предрегистрационные исследования лекарственных средств, которые предназначены для обеспечения их качества, эффективности и безопасности. Также мы обсудим вопросы трансфера технологий и пострегистрационных исследований лекарственных препаратов.
В первой части статьи на основе системного анализа указов Петра I приведены шаги Российского Императора по учреждению и становлению аптечной службы России. Анализ текста указов показал, что особый интерес Петра I к распределению лекарств появился в конце XVII – начале XVIII века, после первого посещения Европы. Первым его шагом, направленным на контроль распределения лекарств, стал Указ таможенной службе о необходимости досмотра и присылке в Москву аптекарских припасов, привозимых из-за границы. Получив контроль над привозом медикаментов и монопольным их распределением, Петр I организует доставку лекарств из царской аптеки в армию. Следующим шагом царя стала организация сети московских аптек. Для этого он издает Указ об организации на Москве восьми аптек. Позже такие аптеки были организованы в Петербурге и других крупных городах России. Владельцам этих аптек Петр I выдает именные грамоты, призванные охранять их от чрезмерных поборов и несправедливости городских властей. Для снабжения появившихся аптек необходимо было наладить их снабжение соответствующим сырьем. Для этого Петр I своими указами распорядился закупать лекарственные травы, собранные в Сибири, организовать в Москве, Петербурге и Астрахани аптечные огороды и ограничить торговлю некоторыми важными товарами. Кроме того, по Указу Петра I отправляются научные экспедиции по России на поиск российской минеральной воды и изучению богатств Сибири.
МЕРОПРИЯТИЯ
С 11 по 14 апреля в МВЦ «Крокус Экспо» состоялась 21-я Международная выставка лабораторного оборудования и химических реактивов «Аналитика Экспо 2023».
ПОИСК И РАЗРАБОТКА НОВЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
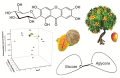
Введение. Ксантоновые гликозиды обладают уникальной структурой и свойствами. Большое количество исследований направлено на поиск производных С-гликозида мангиферина с более высокой биодоступностью. Применение QSAR-анализа позволит оптимизировать направление поиска новых ксантоновых производных с заданными характеристиками.
Цель. Используя доступные дескрипторы химической структуры, физико-химических свойств и биоактивности молекул, проанализировать выборку известных гомологов и аналогов мангиферина с целью QSAR прогнозирования биологического действия новых ксантоновых С-гликозидов.
Материалы и методы. Объектами исследования служили 26 молекул природных гомологов и модифицированных производных мангиферина. С использованием программы ChemicPen построены топологические графы соединений. Для расчета топологического индекса Балабана, обладающего высокой дискриминирующей способностью, применили ПО ChemicDescript. Липофильность молекул (log P), а также критерии правила Липински, рассчитаны в Molinspiration. При помощи Pass Online прогнозирован спектр наиболее вероятной (Pa > 0,7) биологической активности описываемых соединений. Для графического представления полученных результатов использовали ПО Origin (OriginLab, США).
Результаты и обсуждение. Мангиферин и его природные гомологи – наиболее гидрофильные соединения. Гидролиз С-гликозидной связи, алкилирование, ацилирование, введение аминозамещенного радикала в структуру мангиферина приводит к росту липофильных свойств. Спектр наиболее вероятной биологической активности описываемых молекул: противоопухолевое, антиоксидантное и кардиопротективное действие. Результаты ADMET моделирования на основе критериев подобия вещества лекарственному показали, что только 4 соединения соответствуют эмпирическому правилу пяти. Ошибка прогноза, установленная в результате кросс-валидации модели, связывающая индекс Балабана и липофильность соединений с их биоактивностью, составила в среднем не более 3 %.
Заключение. Продемонстрирована взаимосвязь между структурой и свойствами обсуждаемых молекул. Открываются возможности прогнозирования свойств природных и синтетических ксантоновых С-гликозидов и дальнейшего использования полученных результатов для направленного синтеза новых соединений.
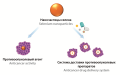
Введение. За последнее время под влиянием стремительного развития нанотехнологий, все большее внимание к использованию в биомедицинских целях, в частности для лечения онкологических заболеваний, привлекают наночастицы селена благодаря своим особым физико-химическим свойствам. В обзоре рассмотрены наночастицы селена, которые широко исследуются в области онкологии.
Текст. Данный обзор посвящен анализу научной литературы по исследованию противораковой активности наночастиц селена в отношении клеточных линий рака человека, а также по исследованию их в качестве системы доставки противоопухолевых препаратов. Кроме этого, обсуждаются механизмы противоопухолевой активности наночастиц селена в отношении злокачественных новообразований.
Заключение. В результате проведенного анализа литературных данных установлено, что наночастицы селена демонстрируют весьма неплохое противоопухолевое действие в отношении различных клеточных линий рака человека. Показано, что противоопухолевая активность наночастиц селена преимущественно связана с индукцией внешних и внутренних сигнальных путей апоптоза, который приводит к гибели раковых клеток. Также наночастицы селена являются перспективными системами для доставки разных противоопухолевых препаратов, обеспечивая высокую эффективность и биодоступность лекарственных средств в опухолевые клетки, а также низкую токсичность в отношении здоровых клеток.
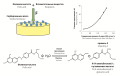
Введение. Поиск новых, эффективных и безопасных фармакологически активных веществ остается актуальной задачей в области фармации. Множество соединений ряда пиперидина, морфолина широко используются в медицинской практике и относятся к важной группе биологически активных соединений. Проведен информационный, литературный поиск по синтезу новых производных пиперидина и морфолина. В статье обобщены результаты исследований новых производных пиперидина и морфолина как потенциальных источников биологически активных веществ.
Текст. Обзор посвящен взаимосвязи между фармакологической активностью N-производных пиперидина и морфолина в отношении различных биологических мишеней и структурой вещества, подчеркивается важность пиперидинового и морфолинового кольца в дизайне и разработке лекарственных препаратов. Пиперидин и морфолин рассматриваются как прерогативные структуры не только для повышения активности, но и для получения биологических веществ с желаемыми терапевтическими свойствами и улучшенной фармакокинетикой.
Заключение. Литературный обзор показывает текущую тенденцию в отношении изучения производных морфолина и пиперидина, раскрывает их высокую фармакофорную активность. Обзор предоставит исследователям необходимую базу знаний для внесения химических структурных изменений в структуры лекарств лидеров для усиления фармакологических активностей.
ФАРМАЦЕВТИЧЕСКАЯ ТЕХНОЛОГИЯ
Введение. Вспомогательные вещества (ВВ) – неотъемлемый компонент лекарственных препаратов (ЛП). В тоже время ВВ, содержащиеся в них примеси и сорбированная вода являются одной из причин деградации активной фармацевтической субстанции (АФС). Такое влияние ВВ особенно важно оценивать для склонных к гидролизу АФС. Фолиевая кислота (ФК) гидролизуется под действием УФ-облучения и основным продуктом разложения является N-(п-аминобензоил)глутаминовая кислота (примесь А). При разработке ЛП «Фолиевая кислота таблетки, покрытые пленочной оболочкой, 1,0 мг» в процессе хранения нами было обнаружено увеличение содержания примеси А. Поскольку таблетки хранились в контурной ячейковой упаковке, состоящей из поливинилхлоридной пленки и алюминиевой фольги, в отсутствии УФ-облучения, причиной гидролиза ФК является состав таблеток и/или параметры процесса их получения.
Цель. Исследовать влияние ВВ, входящих в состав таблеток, и параметры технологического процесса их получения на содержание примеси А в процессе хранения ЛП фолиевой кислоты.
Материалы и методы. Объектами исследования являлись таблетки ФК, содержащие 1,0 мг АФС. Таблетки ФК наработаны по технологии прямого прессования. Усилие прессования варьировали в диапазоне 5–15 кН.
Результаты и обсуждение. Установлено, что при хранении в течении 300 суток таблеток ФК, содержащих 93,0 % моногидрата лактозы, и полученных при усилии прессования выше 10 кН, содержание примеси А в них становится выше предельно допустимого. Возможно, лактоза одновременно выступает как в роли источника свободной воды, так и является катализатором реакции гидролиза ФК. Поскольку взаимодействие лактозы и ФК протекает в твердой фазе, рост давления прессования ускоряет гидролиз АФС за счет увеличения площади контакта частиц и их подвижности. Анализ бинарных смесей ФК с крахмалом, лактозой, микрокристаллической целлюлозой и коповидоном подтвердил, что наибольшее влияние на скорость гидролиза АФС оказывает лактоза.
Заключение. Вероятно, моногидрат лактозы, является основной причиной гидролиза ФК в исследуемых смесях. Независимо от механизма его действия увеличение усилия прессования выше 10 кН приводит к росту скорости гидролиза ФК. Нами был подобран оптимальный диапазон усилия прессования (5–10 кН) для таблеточных смесей, содержащих моногидрат лактозы и ФК.
МЕТОДЫ АНАЛИЗА ЛЕКАРСТВЕННЫХ СРЕДСТВ
Введение. Таурин является непротеиногенной аминокислотой. Молекула участвует в липидном обмене, адсорбирует жирорастворимые витамины, а его конъюгаты с желчными кислотами способствуют эмульгированию жиров в кишечнике. Лекарственные препараты, в состав которых входит молекула таурина обладают антикатарактным, кардиотоническим, метаболическим действием, а также стимулируют регенерацию. Среди лекарственных форм, где в качестве действующего вещества выступает таурин есть твердая лекарственная форма – таблетки, покрытые пленочной оболочкой. Одним из методов оценки качества твердых лекарственных форм является тест сравнительной кинетики растворения. Широко распространенным методом количественно определения в рамках теста растворения является высокоэффективная хроматография с ультрафиолетовым детектированием, однако для таурина, не содержащего хромофорных групп в своей структуре, этот метод на прямую не применим. Для решения данной проблемы можно применить метод предколоночной дериватизации, в результате которой в структуру вводится фрагмент, обеспечивающий батохромный сдвиг в УФ-спектре исходного соединения.
Цель. Разработка, валидация и апробация аналитической методики количественного определения таурина методом высокоэффективной хроматографии с ультрафиолетовым детектированием в рамках проведения теста сравнительной кинетики растворения таблеток таурина дозировкой 250 и 500 мг.
Материалы и методы. Для анализа использовались препараты: таурин таблетки, покрытые пленочной оболочкой 250 мг и 500 мг, отечественного производства с действующим сроком годности. Тест сравнительной кинетики растворения проводили на приборе для теста «Растворение» DT 126 Light (ERWEKA GmbH, Германия). Хроматографическое разделение и детектирование проводили на высокоэффективном жидкостном хроматографе Nexera-i LC-2040 (Shimadzu Corporation, Япония), оснащенном термостатом колонок и образцов, дегазатором, автосамплером и ультрафиолетовым детектором. Детектирование проводилось при длине волны 254 нм после дериватизации молекулы таурина 4-толуолсульфонилхлоридом. Использовали колонку Shim-pack Velox C18 5 μm 4.6 × 150 мм (Shimadzu Corporation, Япония) и предколонку Shim-pack Velox C18 EXP Guard Column Cartridge 5 μm 4.6 × 5 мм (Shimadzu Corporation, Япония). Обработку первичных данных проводили при помощи программного обеспечения LabSolutions Single LC (Shimadzu Corporation, Япония).
Результаты и обсуждение. Подобраны оптимальные условия дериватизации таурина, разработана и валидирована методика количественного определения таурина методом ВЭЖХ-УФ в рамках теста сравнительной кинетики растворения в трёх средах растворения: 0,1 М раствор хлористоводородной кислоты с рН 1,2, ацетатный буферный раствор с рН 4,5, фосфатный буферный раствор с рН 6,8, а также в среде контроля качества – воде очищенной. При проведении валидации разработанной методики установлено, что валидационные характеристики находятся в пределах критериев приемлемости во всех средах растворения. Аналитический диапазон методики составил 0,05–1,2 мг/мл и позволяет применять разработанную методику для количественного определения в рамках теста сравнительной кинетики растворения таблеток с дозировкой 250 мг и 500 мг.
Заключение. Методика была апробирована в трех средах растворения: 0,1 М раствор хлористоводородной кислоты с рН 1,2, ацетатный буферный раствор с рН 4,5, фосфатный буферный раствор с рН 6,8, а также в среде контроля качества – воде очищенной. Во всех средах наблюдалось полное высвобождение у обеих дозировок (более 85 % к 30 минуте).
Введение. Щавель приморский (Rumex maritimus L., Polygonaceae) используется как лекарственное и пищевое растение в странах Азии. Растение содержит биологически активные вещества (БАВ) различных классов: флавоноиды, дубильные вещества, антрахиноны и др. Извлечения из растения проявляют антибактериальную, антиоксидантную, противовоспалительную, вяжущую активность, обладают противодиабетическим потенциалом. Растение является однолетником, поэтому большая часть биологически активных веществ накапливается в надземных органах. Важной задачей является стандартизация сырья щ. приморского и разработка нормативной документации для его внедрения в медицинскую практику.
Цель. Провести фитохимический анализ надземной части щ. приморского.
Материалы и методы. Для получения извлечений использовали высушенную надземную часть щ. приморского, а также отдельные высушенные надземные органы (листья, цветки, плоды, стебли). Качественный анализ извлечений проводили с использованием метода обращенно-фазовой ВЭЖХ. Относительное содержание компонентов смеси вычисляли методом простой нормировки. Суммарное содержание свободных антрахинонов и антрагликозидов определяли спектрофотометрическим методом в пересчете на хризофановую кислоту после проведения кислотного гидролиза. Количественное определение танинов проводили титриметрическим методом.
Результаты и обсуждение. В надземной части щ. приморского впервые обнаружены флавоноиды изокверцетин, авикулярин. Доминирующим компонентом сырья является рутин. Среди антраценпроизводных преобладает хризофанол. Наиболее высокая концентрация антрахинонов (2,80 ± 0,04 %) обнаружена в цветках. Дубильные вещества накапливаются преимущественно в листьях (9,97 ± 0,02 %). Значительное количество дубильных веществ (6,60 ± 0,03 %) и антраценпроизводных (1,96 ± 0,03 %) содержится в траве.
Заключение. Фитохимический анализ надземной части щ. приморского показал присутствие значительного количества антрахинонов. В качестве сырья предлагается использовать траву щ. приморского в стадии цветения. Предлагается проводить стандартизацию сырья по антраценпроизводным в пересчете на хризофановую кислоту (не менее 1,5 %).
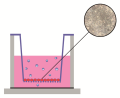
Введение. Растровая электронная микроскопия – современный метод, позволяющий изучить не только морфологические особенности объектов, но и провести микрорентгеноструктурный анализ. В настоящее время метод активно внедряется в изучение биологических объектов (включая растительные). Облепихи крушиновидной (Hippophaë rhamnoides L.) листья являются нефармакопейным видом лекарственного растительного сырья. Дальнейшее изучение особенностей морфологии, анатомии и фитохимического состава листьев может способствовать получению новых, в том числе и комбинированных, лекарственных средств, что потребует разработки фармакопейной статьи на данное лекарственное растительное сырье.
Цель. Целью исследования являлось изучение морфолого-анатомических признаков облепихи крушиновидной листьев методом растровой электронной микроскопии.
Материалы и методы. Объектом исследования служили высушенные цельные листья облепихи крушиновидной (Hippophaë rhamnoides L.), собранные в Воронежской области в 2021 году в период массовой зрелости плодов. Для проведения исследования методом растровой электронной микроскопии кусочки листьев предварительно напыляли золотом на автоматической напылительной установке Q150R ES (Quorum Technologies Ltd., Великобритания) для повышения проводимости. Микрофотографии получены на электронном микроскопе JSM-6510LV (JEOL Ltd., Япония).
Результаты и их обсуждение. Проведено изучение морфологии, некоторых особенностей анатомического строения облепихи крушиновидной листьев и уточнены основные микродиагностические признаки (характер поверхности, типы трихом, наличие устьиц). Установлено содержание элементов (кремния, калия, алюминия, углерода и кальция) при проведении микрорентгеноструктурного анализа. Получены микрофотографии пыльцевых зерен растения, установлено присутствие в них элемента железа.
Заключение. Впервые использован метод растровой электронной микроскопии для изучения морфолого-анатомических признаков облепихи крушиновидной листьев. Уточнены основные диагностические признаки листьев и их расположение. Установлено, что в составе элементов сырья преобладает углерод, а также накапливается кальций. Предположено накопление алюминия, кремния и калия в многочисленных волосках, густо покрывающих верхнюю, и особенно нижнюю, поверхности листовой пластинки. Установлена морфология поверхности пыльцевых зерен облепихи крушиновидной, имеющих шарообразную форму с шиповатой оболочкой. Для пыльцевых зерен, кроме углерода, характерно накопление железа и кремния.
Введение. Белок резистентности рака молочной железы (BCRP) является эффлюксным мембранным транспортером, контролирующим фармакокинетику большого числа лекарственных средств. Его активность может изменяться на фоне приема ряда эндо- и экзогенных веществ, таким образом, делая его звеном межлекарственных взаимодействий.
Цель. Цель исследования – разработка методики тестирования лекарственных веществ на принадлежность к субстратам и ингибиторам BCRP in vitro.
Материалы и методы. Работа выполнена на клетках Сасо-2 гиперэкспрессирующих BCRP; культивирование проводили в трансвелл-системе, состоящей из апикальной и базолатеральной камер. На дно апикальной камеры (полупроницаемая мембрана) высеивали клетки. Оценивался транспорт субстратов BCRP: метотрексата, митоксантрона и кверцетина в концентрациях 1–50 мкМ в направлении из базолатеральной камеры в апикальную (Papp b-a) и в обратном направлении (Papp a-b). Отношение Papp b-a / Papp a-b более «2» характеризует участие транспортера в переносе веществ. Для подтверждения участия BCRP в транспорте тест-субстратов эксперимент проводился с добавлением в камеры ингибитора транспортера – резерпина (50 мкМ). Концентрацию субстратов определяли методом ВЭЖХ-МС/МС.
Результаты и их обсуждение. При добавлении метотрексата (1 мкМ), митоксантрона (1 мкМ) и кверцетина (1−10 мкМ) в обе камеры их содержание в камере-реципиенте не детектировалось. При концентрации метотрексата 5 мкМ отношение Papp b-a / Papp a-b составило 3,38 ± 0,08, что свидетельствует об участии транспортера в его переносе. При концентрации вещества (10 и 50 мкМ) Papp b-a / Papp a-b снижалось до значений ниже «2». При концентрации митоксантрона 5 мкМ Papp b-a / Papp a-b составило 2,72 ± 0,16. Увеличение концентрации до 10 мкМ привело к росту Papp b-a / Papp a-b до 6,18 ± 0,08. При содержании вещества 50 мкМ показатель снижался, но оставался выше значения 2. В концентрации кверцетина 50 мкМ Papp b-a / Papp было ниже «2». Резерпин снижал Papp b-a / Papp a-b метотрексата в 3,31 раза (p = 0,0002), что свидетельствует об устранении асимметрии транспорта вещества. При концентрации митоксантрона 10 мкМ резерпин снижал его Papp b-a / Papp a-b в 3,36 раза (p < 0,0001). Результаты свидетельствуют об участии BCRP в контроле переноса обоих веществ через клеточный монослой.
Заключение. Разработана и апробирована на клетках линии Caco-2 методика тестирования лекарственных средств на принадлежность к субстратам и ингибиторам BCRP с использованием в качестве маркерных субстратов метотрексата (5 мкМ) и митоксантрона (10 мкМ), а в качестве ингибитора – резерпина (50 мкМ).
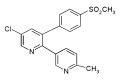
Введение. Эторикоксиб – селективный ингибитор циклооксигеназы (ЦОГ-2), применяемый для лечения острой боли и обладающий противовоспалительной и анальгетической эффективностью. Эторикоксиб вызывает меньшее количество осложнений по сравнению с другими нестероидными противовоспалительными препаратами (НПВП). ФБУ «ГИЛС и НП» была разработана глазная жидкая лекарственная форма на основе эторикоксиба. В настоящей статье предложена методика определения содержания эторикоксиба в жидкой лекарственной форме методом высокоэффективной жидкостной хроматографии с УФ-детектированием.
Цель. Разработка и валидация методики количественного определения эторикоксиба в жидкой лекарственной форме.
Материалы и методы. Для анализа использовали глазные капли с концентрацией действующего вещества эторикоксиба 0,05 %, стандартный образец эторикоксиб (Kekule Pharma Limited, Индия, серия ACE-3 WS001/15). Хроматографическое разделение проводили на высокоэффективном жидкостном хроматографе Agilent 1220 Infinity II LC (Agilent Technologies, США), оснащенном градиентным насосом, термостатом колонок и детектором с диодной матрицей. Анализ проводили на колонке Kromasil С8 250 × 4,6 мм, используя в качестве подвижной фазы ацетонитрил и 0,05 М буферный раствор дигидрофосфата калия рН = 4,2 в соотношении 46 : 54. Время анализа составило 15 минут при длине волны детектирования 235 нм.
Результаты и обсуждение. Разработана и проведена валидация методики количественного определения эторикоксиба в жидкой лекарственной форме по следующим показателям специфичность, линейность, правильность, промежуточная (внутрилабораторная) прецизионность, повторяемость.
Заключение. По результатам валидационных испытаний все перечисленные параметры соответствуют критериям приемлемости. Предлагаемая методика характеризуется высокой эффективностью и специфичностью.
Введение. Образование и накопление биологически активных веществ в растениях – сложный процесс, связанный с рядом факторов окружающей среды, в том числе антропогенных. Изучение особенностей качественного состава эфирного масла травы полыни горькой различных с экологической точки зрения мест заготовки является актуальным.
Цель. Цель исследования – изучение качественного состава эфирного масла травы полыни горькой, заготовленной в различных с экологической точки зрения районах Воронежской области.
Материалы и методы. В Воронежском регионе было выбрано 4 точки заготовки сырья, разнообразных с точки зрения антропогенного воздействия. Выделение эфирного масла из сырья проводили по методике ФС «Полыни горькой трава». Определение компонентного состава полученных эфирных масел проводили на хромато-масс-спекрометрическом комплексе Agilent 7890B GC System (Agilent Technologies, США) с масс-селективным детектором Agilent 5977A MSD (Agilent Technologies, США). Анализ и обработка данных осуществлялись на основании баз данных NIST11 (от 19.05.2011), использовалось программное обеспечение MassHunter ver. B.06.00 и NIST MS Search ver. 2.0.
Результаты и обсуждение. В образце эфирного масла, полученного из заповедного сырья, на долю монотерпеновых соединений приходится более 82 %, а сесквитерпеновых соединений – 16,6 %, около 2 % составляют примеси органической природы. Интенсивный биосинтез монотерпенов отмечен в образце, собранном в районе сельскохозяйственных полей Верхнехавского района, его массовая доля – более 73 %. В образцах сырья, имеющих антропогенную нагрузку (ОАО «Минудобрения» и автомобильная трасса М4), доля монотерпеновых соединений значительно ниже (соответственно 63,7 и 49 %). Рост доли сесквитерпеновых соединений в последних образцах эфирного масла полыни, возможно, связан с избыточной кислотностью урбанизированных мест заготовки. Сесквитерпеновое соединение хамазулен, окрашивающий эфирное масло в голубой цвет, определен только в двух образцах полыни горькой травы, заготовленных вдоль сельскохозяйственных полей и в трассы М4, что объясняет наличие голубого оттенка в этих маслах.
Заключение. Хромато-масс-спектрометрический анализ эфирного масла исследуемых образцов травы полыни горькой позволил идентифицировать в них более 70 различных компонентов, при этом качественный состав эфирного масла сырья различных мест заготовки заметно отличался, что может указывать на значительное влияние места произрастания вида и антропогенных факторов на особенности вторичного метаболизма терпеновых соединений в растительном организме.
Введение. Микроэлементы являются неотъемлемой частью организма человека, однако около 80 % населения отмечает дисбаланс их содержания. В лекарственных растениях минеральные вещества находятся в легко доступной и усвояемой форме вместе с биологически активными веществами. Весьма популярны для профилактики и в составе комплексной терапии различных заболеваний лекарственные растительные сборы. Однако сведения о содержании микроэлементов в многокомпонентных лекарственных растительных препаратах весьма ограничены. Поэтому необходимы исследования минерального состава, которые позволят рассматривать растительные сборы в качестве дополнительного источника микроэлементов.
Цель. Изучить содержание микроэлементов (B, Si, Al, Ba, Sr, Ti) в грудном сборе № 4, его компонентах и водных извлечениях из них.
Материалы и методы. Объектами исследования были грудной сбор № 4, его отдельные компоненты и водные извлечения из них. Настои из образцов получали согласно инструкции по применению на упаковке лекарственного растительного препарата. Подготовку проб к анализу осуществляли смесью концентрированной азотной кислоты и воды деионизированной в микроволновой системе Milestone Ethos Up (Milestone, Италия). Анализ проводили методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой на приборе ИСП-АЭС 720-ES (Agilent Technologies, США).
Результаты и обсуждение. Обнаружено, что концентрации Si, Al, B, Sr, Ba, Ti в отдельных компонентах сбора варьировали в диапазоне 2,9–1240 мг/кг, переход микроэлементов в водные извлечения составил 0,4–34,2 %. Содержание этих элементов в грудном сборе № 4 найдено 13,3–920,7 мг/кг, а степень извлечения в настой составила 3–40 %. Сравнительный анализ показал, что извлечение B, Al, Ba из сбора в настой на 14–58 % выше, чем из отдельных компонентов, входящих в его состав. Установлено, что с настоем из грудного сбора № 4 в организм человека поступает 50 % бора и 264 % кремния от рекомендуемого адекватного уровня потребления в РФ.
Заключение. Проведенное исследование показало, что грудной сбор № 4 можно рассматривать как дополнительный источник B и Si в организм человека. Концентрации Al, Sr, Ba, Ti находились в пределах средних значений диапазона содержания этих элементов в растениях.
Введение. В настоящее время биосимиляры обрели довольно широкое применение в терапии ряда хронических и опасных для жизни заболеваний. Благодаря им происходит значительное снижение экономического давления биологических препаратов на систему здравоохранения и обеспечивается широкая доступность пациентов к эффективным и безопасным лекарственным средствам. Одним из важнейших этапов доказательства биосимилярности является проведение физико-химической и функциональной характеризации белков. Данный комплекс исследований является общепринятым, максимально чувствительным и позволяет дать заключение о соответствии биосимиляра оригинальному препарату.
Цель. Проведение физико-химической и функциональной характеризации препарата Ринсулин® Р (GP40051) в сравнении с оригинальным препаратом Хумулин® Регуляр.
Материалы и методы. Первичная структура была исследована методами высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием и матрично-активированной лазерной десорбции/ионизации. Идентичность более высоких белковых структур была доказана методами кругового дихроизма, капиллярного изофокусирования, спектрометрии и динамического рассеяния света. Сопоставимость профилей примесей препаратов оценивали при помощи методов эксклюзионной хроматографии и обращенно-фазовой высокоэффективной жидкостной хроматографии. Функциональная характеризация включала в себя метаболический клеточный тест «захват глюкозы» и анализы связывания с рецептором инсулина (кинетика связывания с рецепторами типа А и В, фосфорилирование инсулинового рецептора).
Результаты и обсуждение. В ходе данной работы была показана идентичность физико-химических и функциональных характеристик GP40051. Между препаратом сравнения GP40051 и референтным препаратом Хумулин® Регуляр было продемонстрировано полное совпадение первичной последовательности, структур высокого порядка и профилей примесей. Функциональные исследования показали, что GP40051 и Хумулин® Регуляр обладают одинаковой активностью.
Заключение. По результатам исследования подтверждена аналитическая биосимилярность препарата Ринсулин® Р (GP40051) оригинальному препарату Хумулин® Регуляр, что обеспечило научную основу для проведения специально разработанной клинической программы, и явилось основанием для регистрации в РФ.
ДОКЛИНИЧЕСКИЕ И КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Введение. В настоящее время предполагается, что вирус SARS-CoV-2 (severe acute respiratory syndrome-related coronavirus 2), вызывающий новую коронавирусную инфекцию COVID-19 (Coronavirus Disease 2019) останется постоянной глобальной угрозой. В связи с этим, вопрос разработки лекарственных препаратов для лечения COVID-19 остается актуальным. Комбинация нирматрелвира с ритонавиром обладает прямым противовирусным действием: при ее применении удается повысить эффективность терапии и снизить риск осложнений COVID-19. Разработка и валидация методики совместного определения нирматрелвира и ритонавира в плазме крови человека является необходимой задачей для проведения аналитической части клинического исследования с целью дальнейшего изучения фармакокинетических параметров.
Цель. Целью исследования является разработка и валидация методики совместного определения нирматрелвира и ритонавира в плазме крови человека методом высокоэффективной жидкостной хроматографии с тандемным масс-селективным детектированием (ВЭЖХ-МС/ МС) для дальнейшего изучения фармакокинетики.
Материалы и методы. Определение нирматрелвира и ритонавира в плазме крови человека проводили методом ВЭЖХ-МС/МС. В качестве пробоподготовки был использован способ осаждения белков ацетонитрилом. Внутренний стандарт: прометазин. Подвижная фаза: 0,1%-й раствор муравьиной кислоты в воде (элюент А), 0,1%-й муравьиной кислоты в ацетонитриле (элюент В). Колонка: Phenomenex Luna C18 50 × 2,0 мм, 5 мкм. Аналитический диапазон методики: 50,00–10000,00 нг/мл для нирматрелвира, 5,00–1000,00 нг/мл для ритонавира в плазме крови. Источник ионизации и ионизация: электроспрей, положительная. Условия детектирования: 499,90 → 110,10 m/z, 499,90 → 319,20 m/z (нирматрелвир), 720,90 → 426,00 m/z, 720,90 → 296,20 m/z, 720,90 → 268,10 m/z, 720,90 → 197,10 m/z, 720,90 → 139,90 m/z (ритонавир), 285,15 → 198,05 m/z (прометазин).
Результаты и обсуждение. Разработанная методика была валидирована по следующим валидационным параметрам: селективность, эффект матрицы, калибровочная кривая, точность, прецизионность, степень извлечения, нижний предел количественного определения перенос пробы, стабильность.
Заключение. Разработана и валидирована методика совместного определения нирматрелвира и ритонавира в плазме крови человека методом ВЭЖХ-МС/МС. Подтвержденный аналитический диапазон методики составил 50,00–10000,00 нг/мл для нирматрелвира, 5,00– 1000,00 нг/мл для ритонавира в плазме крови. Полученный аналитический диапазон позволяет применять разработанную методику для проведения фармакокинетических исследований комбинированных препаратов нирматрелвира и ритонавира.
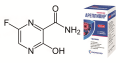
Введение. Новая коронавирусная инфекция COVID-19 (Coronavirus Disease 2019) вызвана оболочечным вирусом с одноцепочечной РНК позитивной полярности – SARS-CoV-2 (severe acute respiratory syndrome-related coronavirus 2). Одним из противовирусных препаратов, рекомендованных для этиотропного лечения COVID-19, является фавипиравир. Парентеральное введение препарата имеет ряд преимуществ по сравнению с другими способами введения: отсутствует взаимодействие с пищей и пищеварительными ферментами, возможно применение для пациентов c заболеваниями пищеварительной системы и пациентов без сознания. В России для парентерального применения зарегистрирован препарат «Арепливир» с действующим веществом фавипиравир.
Цель. Целью исследования является изучение фармакокинетики препарата «Арепливир», лиофилизат для приготовления концентрата для приготовления раствора для инфузий (АО «Биохимик», Россия), держатель регистрационного удостоверения ООО «ПРОМОМЕД РУС», при внутривенном капельном введении здоровым добровольцам в рамках фазы I клинического исследования.
Материалы и методы. Клинический, аналитический этапы исследования, анализ фармакокинетических параметров проводился в рамках исследования различных доз препарата «Арепливир», лиофилизат для приготовления концентрата для приготовления раствора для инфузий (ООО «ПРОМОМЕД РУС», Россия). Хроматографическое разделение и детектирование проводили на высокоэффективном жидкостном хроматографе LC-2040С (Shimadzu Corporation, Япония) с встроенным УФ-детектором, четырехкомпонентным градиентным насосом низкого давления, дегазатором, автосамплером, термостатом колонок и контроллером (Shimadzu Corporation, Япония). Расчет фармакокинетических параметров проводился с помощью Microsoft Excel с расширением для проведения фармакокинетического анализа Boomer (Department of Pharmacokinetics and Drug Metabolism, Allergan, Irvine, CA 92606, США). Описательная статистика фармакокинетических параметров рассчитывались с помощью IBM SPSS Statistics (версия 23.0), IBM, США. Корреляционно-регрессионный анализ проводился с помощью Microsoft Excel (Microsoft Corporation, США).
Результаты и обсуждение. Для доз 400, 800, 1600 и 1800 мг при однократном введении в 4 когортах по 5 добровольцев рассчитаны фармакокинетические параметры. Для максимального значения концентрации фавипиравира (Сmax) от вводимой дозы установлена статистически значимая прямая корреляционная связь весьма высокой тесноты по шкале Чеддока (r = 0,98; p = 0,02; r – коэффициент корреляции Пирсона; p – достигнутый уровень значимости) и статистическая значимость коэффициента детерминации (R2 = 0,96; F = 45,97; p = 0,02; R2 –коэффициент детерминации; F – фактическое значение критерия Фишера). Для площади под кривой «плазменная концентрация – время» с момента введения препарата до последней определяемой концентрации во временной точке t (AUC0-t) от вводимой дозы установлена статистически значимая прямая корреляционная связь весьма высокой тесноты по шкале Чеддока (r = 0,97; p = 0,03) и статистическая значимость коэффициента детерминации (R2 = 0,94; F = 33,54; p = 0,03). Полученные результаты позволяют говорить о линейности Cmax и AUC0-t на всем изучаемом диапазоне доз (400–1800 мг).
Заключение. По полученным на аналитическом этапе исследования значениям концентраций фавипиравира были рассчитаны фармакокинетические параметры, построены усредненные фармакокинетические профили в линейных и полулогарифмических координатах после однократного введения различных доз препарата «АРЕПЛИВИР», лиофилизат для приготовления концентрата для приготовления раствора для инфузий (ООО «ПРОМОМЕД РУС», Россия). Установлена линейность Cmax и AUC0-t от вводимой дозы препарата «Арепливир» на всем изучаемом диапазоне доз (400–1800 мг) при однократном введении. Полученные результаты определяют возможность дальнейшего изучения режима дозирования с многократным введением фавипиравира, а также позволяют осуществить переход к последующим фазам клинических исследований препарата «Арепливир».
Введение. Создание инновационного высокоэффективного и конкурентоспособного лекарственного препарата является долгим и дорогостоящим процессом, результат которого достаточно сложно спрогнозировать заранее. Для ускорения выхода нового препарата на рынок и снижения материальных затрат разработчика целесоообразным является включение доклинических экспериментов непосредственно в процесс лабораторной фармацевтической разработки.
Текст. Цель настоящей работы заключается в создании обоснованного подхода к осуществлению лабораторной фармацевтической разработки с привлечением исследований in vivo. Включение доклинических исследований в процесс лабораторной фармацевтической разработки позволит исключить негативное влияние фармацевтических факторов на биодоступность лекарственного средства (ЛС), избежать ошибок при выборе вспомогательных веществ (ВВ), а также снизить материальные и временные затраты. Перечисленные в обзоре примеры, демонстрирующие актуальность проведения доклинических экспериментов на разных этапах лабораторной фармразработки, позволили описать более четкий алгоритм действий при осуществлении лабораторной фармацевтической разработки нового лекарственного препарата с момента выбора молекулы-кандидата в ЛС.
Заключение. Для повышения вероятности успешности фармацевтической разработки на этапе выбора лекарственной формы и ее состава необходимо проведение экспериментов по изучению фармакокинетики и/или фармакодинамики, что позволит разработать лекарственный препарат с оптимальным фармакокинетическим профилем, снизить количество доклинических исследований, стоимость разработки и обеспечить успешную трансляционность данных в клиническую практику.
Введение. Обзор научной литературы показал, что существующие стандарты оценки качества лекарств не включают оценку осмотической активности лекарственных растворов и их местное раздражающее действие на ткани в местах подкожных, внутримышечных и внутривенных инъекций. Поэтому в настоящее время растворы для инъекций, считающиеся качественными, могут не иметь изотоническую активность и высокую постинъекционную безопасность.
Текст. Изучение диапазона величины концентрации качественных лекарственных растворов, готовых для инъекции, показало, что допустимая величина концентрации основных ингредиентов находится в диапазоне 0,01 – 76 %. Проведенное прямое измерение с помощью осмометра величины осмотической активности лекарственных растворов для инъекций, считающихся сегодня качественными, показало, что растворы для инъекций могут иметь гипотоническую, изотоническую и гипертоническую активность, и их осмотическая активность может находится в диапазоне 0 – 3900 мосмоль/л воды. Исследование кислотной активности лекарственных растворов показало, что в соответствии с фармакопейными требованиями качества лекарств современные качественные лекарственные растворы, готовые для инъекции, могут иметь кислую, нейтральную или щелочную активность. Установлено, что растворы, имеющие гипертоническую активность, обладают местным раздражающим действием. Причем увеличение гипертонической активности лекарственных растворов увеличивает их местное раздражающее действие. Обнаружено, что чрезмерно большая гипертоническая активность лекарственных растворов может являться причиной развития локального постинъекционного осложнения, известного под названием «синдром Николау», причина которого длительное время оставалась неизвестной. Синдром Николау включает локальный болевой синдром, асептическое воспаление, некроз и абсцесс.
Заключение. Авторы провели анализ литературы, результаты которого позволили сделать выводы и предположения. Растворы, содержащие лекарственные средства в концентрации более 10 %, могут иметь наиболее высокую гипертоническую активность, которая может стать причиной чрезмерно сильного обезвоживающего, местного раздражающего и прижигающего действия. Поэтому инъекции таких лекарств наиболее опасны развитием постинъекционных некрозов и абсцессов. Именно поэтому разведение концентрированных лекарственных растворов в 2–10 раз водой или раствором 0,25%-го новокаина повышает безопасность инъекций. Предлагается внести данную рекомендацию в инструкцию по медицинскому применению высококонцентрированных лекарственных растворов и включить оценку осмотической активности и местного раздражающего действия лекарственных растворов в стандарт контроля качества лекарств.
Введение. Одним из наиболее прогрессирующих направлений современного этапа развития биологии является углубление знаний о механизмах регуляции метаболических процессах, в частности о сигнальных молекулах, которые передают информацию клетке через ионные каналы и рецепторы ядерные, связанные с G-белком или с ферментативной активностью. Ядерный рецептор Farnesoid X receptor (FXR) в основном экспрессируется в печени и кишечнике, он регулирует ключевые гены, обеспечивающие процессы синтеза, транспорта и реабсорбции желчных кислот, а также участвует в метаболизме липидов и углеводов.
Цель. Оценить влияние агониста фарнезоидного Х-рецептора на постпрандиальную липемию у крыс, получающих рацион, содержащий супрафизиологическую дозу жиров.
Материалы и методы. Проведено экспериментальное проспективное контролируемое «неослепленное» рандомизированное исследование по изучению влияния агониста фарнезоидного Х-рецептора (обетихолевой кислоты) на постпрандиальную липемию у крыс, получающих рацион, содержащий супрафизиологическую дозу жиров.
Результаты и обсуждение. Показано, что при оценке постпрандиальной липемии достаточно высокую информативность имеет пероральный тест на толерантность к супрафизиологическим дозам жира с определением исходных показателей липидного профиля и через 4 часа после нагрузки. Выявлено, что у животных, которые в течение 28 дней получали рацион, содержащий повышенное количество жира, наблюдался дисбаланс метаболизма липидов с активацией их всасывания в кишечнике, но «замедленной» реакцией механизмов промежуточного обмена липидов, что сопровождалось накоплением в крови голодных крыс триглицеридов, холестерина хиломикронов и ЛПНП. Через 4 часа после кормления у этих животных наблюдалось сверхнормальное повышение триглицеридов и холестерина.
Заключение. Применение обетихолевой кислоты гармонизирует липидный обмен на фоне алиментарной жировой нагрузки за счет активации фарнезоидных Х-рецепторов кишечника и печени, что проявляется одновременным увеличением интенсивности процессов всасывания липидов и их промежуточного обмена. В результате исключается риск возникновения гиперхиломикронемии, гиперхолистеринемии и гипертриглицеридемии, снижается вероятность развития вторичной гиперлипедемии, толерантности к инсулину и функциональной перегрузки (или патологии) печени.
Введение. Радиорезистентность раковых клеток серьезная проблема при лучевой терапии опухолевых заболеваний. Радиосенсибилизирующие препараты делают злокачественные клетки более чувствительными к излучению и повышают эффективность лучевой терапии, однако их широкое клиническое применение ограничено существенными побочными эффектами. Разработка и изучение новых радиосенсибилизаторов представляется актуальной задачей современной фармакологии.
Цель. Целью данной работы было изучение эффективности аскорбата лития в качестве радиосенсибилизатора при воздействии фотонного и нейтронного излучения в широком диапазоне доз.
Материалы и методы. Оценка биологического действия выполнялась на опухолевой линии аденокарциномы рака предстательной железы PC-3. В качестве генераторов ионизирующего излучения использовался циклотрон для получения нейтронного потока и источник кобальт-60 для получения гамма-излучения.
Результаты и обсуждение. Доказано усиление цитотоксического эффекта при сочетанном применении разных видов ионизирующих излучений и аскорбата лития. Выявлена устойчивость лини рака предстательной железы к гамма-излучению в поглощенной дозе 0,5–3,0 Гр. Показано, что опухолевые клетки рака предстательной железы более чувствительны к воздействию исследуемого препарата в минимальных концентрациях в сочетании с нейтронным облучением в сравнении с гамма-излучением в одинаковой поглощенной дозе. Основной механизм радиосенсибилизирующего действия аскорбата лития заключается в локальной индукции окислительного стресса, синергетически усиливающий действие ионизирующего излучения.
Заключение. Сочетание аскорбата лития с нейтронным излучением приводит к более выраженному результирующему цитотоксическому эффекту. Повышение концентрации аскорбата лития приводило к нарастанию прооксидатного эффекта с усилением повреждающего действия на клетки.
Введение. «Трастузумаб» – препарат специфической анти-HER2 терапии одного из самых распространенных типов онкологических заболеваний – рака молочной железы. Несмотря на то, что препарат давно представлен на фармацевтическом рынке, дальнейшее совершенствование связанных с ним аналитических методик остается актуальным в первую очередь в свете разработки и исследования действия биоаналогов. Для трастузумаба одной из возможных нежелательных реакций со стороны иммунной системы является иммуногенность – выработка противолекарственных антител к препарату, в том числе нейтрализующих антител, которые могут влиять на эффективность и профиль безопасности препарата.
Цель. Разработка и валидация методики определения нейтрализующих антител к трастузумабу в сыворотке крови человека.
Материалы и методы. Определение нейтрализующих антител к трастузумабу проводилось с помощью метода конкурентного иммуноферментного анализа, с использованием фотометрического детектирования в видимом диапазоне спектра.
Результаты и обсуждение. Разработанная методика была валидирована по показателям: предел исключения, чувствительность, селективность, специфичность, прецизионность и стабильность (краткосрочная и долгосрочная). Для снижения интерференции компонентов биологической матрицы в анализе на этапе разработки было определено значение минимального необходимого разбавления (1 : 200). Рассчитанное значение предела исключения составило 14,62 %. Чувствительность разработанной методики составила 1985,2 нг/мл нейтрализующих антител к трастузумабу.
Заключение. Полученные при валидации методики результаты позволяют применять методику определения нейтрализующих антител к трастузумабу в сыворотке крови человека оценки иммуногенности препаратов трастузумаба при проведении клинических исследований биоаналогичности.
РЕГУЛЯТОРНЫЕ ВОПРОСЫ
Введение. Обеспечение качественными, эффективными и безопасными лекарственными препаратами, предназначенными для лечения редких (орфанных) заболеваний среди населения государств-членов Союза, является одним из значимых и перспективных векторов развития для производителей-разработчиков. Обеспечение доступности лекарственными препаратами (ЛП) для пациентов, страдающих редкими заболеваниями, должно регулироваться путем государственного стимулирования разработки и вывода на рынок орфанных препаратов у отечественных производителей за счет актуализации и своевременного обновления нормативно-правовых актов в сфере регистрации ЛП, а также предоставления льгот при инициировании процесса регистрации.
Текст. В статье оценивались возможности и перспективы вывода в обращение орфанных лекарственных препаратов в рамках Евразийского экономического союза для отечественных производителей.
Заключение. Обзор возможностей и перспектив вывода в обращение орфанных лекарственных препаратов для отечественных производителей говорит о необходимости развития нормативно-правового регулирования аспектов фармацевтической разработки для повышения доступности лечения пациентов с редкими заболеваниями как на уровне РФ, так и в рамках правового поля Евразийского экономического пространства.
ДИСКУССИИ
Введение. В практику разработки лекарственных препаратов все полнее внедряются методы компьютерной химии, в частности нековалентный молекулярный докинг. Ранее для данного сравнительно молодого инструмента научных исследований не применяли подход управления рисками потенциальных ошибок.
Цель. Создание системы оценки риска ошибки для нековалентного молекулярного докинга.
Материалы и методы. Разработка системы по оценке риска ошибки базировалась на ведущих мировых практиках по нековалентному молекулярному докингу.
Результаты и обсуждения. В результате дедуктивного анализа процесса молекулярного докинга установили области возникновения ошибок и предложили риск-ориентированный алгоритм, который апробировали на выборке статей, полученной в ходе систематического обзора. Выявлена тенденция к частому ограниченному предоставлению информации по методологии расчетного эксперимента, а также по применению практик доказанно ведущих к нерелевантным результатам молекулярного докинга.
Заключение. Полученные данные нельзя экстраполировать на все исследования, ссылающиеся на результаты молекулярного моделирования, однако посредством предложенного риск-ориентированного алгоритма внимание исследователей фокусируется на оценке качества подобных публикаций. Авторы надеются, что разработанный инструмент по оценке риска ошибки в нековалентном молекулярном докинге будет доработан и в итоге внедрен в практику, благодаря чему удастся снизить долю некачественных работ в области разработки лекарственных препаратов на самых ранних этапах.
МАТЕРИАЛЫ КОНФЕРЕНЦИЙ
Введение. Настоящая публикация представляет собой материалы традиционной научной конференции студентов старших курсов Института фармации Сеченовского университета и факультета фундаментальной медицины МГУ им. М. В. Ломоносова под общим девизом «Drug. Лекарство или… сложности перевода», которая состоялась 27 мая 2022 года. Каждый год темой такой конференции становятся самые актуальные медико-социальные проблемы, связанные с эффективностью и безопасностью лекарств. Данная конференция была приурочена к проходившему в это время Х Юбилейному международному междисциплинарному конгрессу по заболеваниям органов головы и шеи, и посвящена проблеме фармакотерапии онкологических заболеваний.
В России, как и в мире, онкологические заболевания широко распространены и занимают второе место среди причин смертности. Так, согласно статистическим данным, каждый 40-й человек в России имеет онкологическое заболевание.
Тысячи исследователей во всем мире стремятся понять этиологию рака, повысить эффективность диагностики и лечения заболевания, обеспечивая медленный, но неуклонный прогресс в решении этих проблем.
Ранняя диагностика и своевременное целенаправленное лечение являются залогом успешной терапии и благоприятного исхода.
В прозвучавших докладах были рассмотрены основные направления создания противоопухолевых лекарственных препаратов, обеспечивающих большую эффективность и безопасность лечения, современные подходы к ранней диагностике рака с помощью микроРНК как маркеров опухоли. Большой интерес вызвало сообщение о возможности предсказания токсичности препаратов еще до стадии химического синтеза на основании компьютерного драг-дизайна. Также было уделено внимание проблемам паллиативного лечения и реабилитации онкологических пациентов, психологическим, этическим и юридическим аспектам этого. Обсуждение и медицинская оценка этих вопросов безусловно вызовет интерес достаточно широкой аудитории. Далее приведены лишь три сообщения из прозвучавших, дающие представление о «классических» методах, новом направлении в лечении, и технологической реализации таргетной терапии опухоли.
ИСПРАВЛЕНИЯ
Разработка и регистрация лекарственных средств. 2022;11(2):59–64. https://doi.org/10.33380/2305-2066-2022-11-2-59-64. Статья опубликована: 25.05.2022.
ISSN 2658-5049 (Online)